Penjelasan Mengenai Kalorimetri ( Termokimia Part Iv ) JUARA SATU
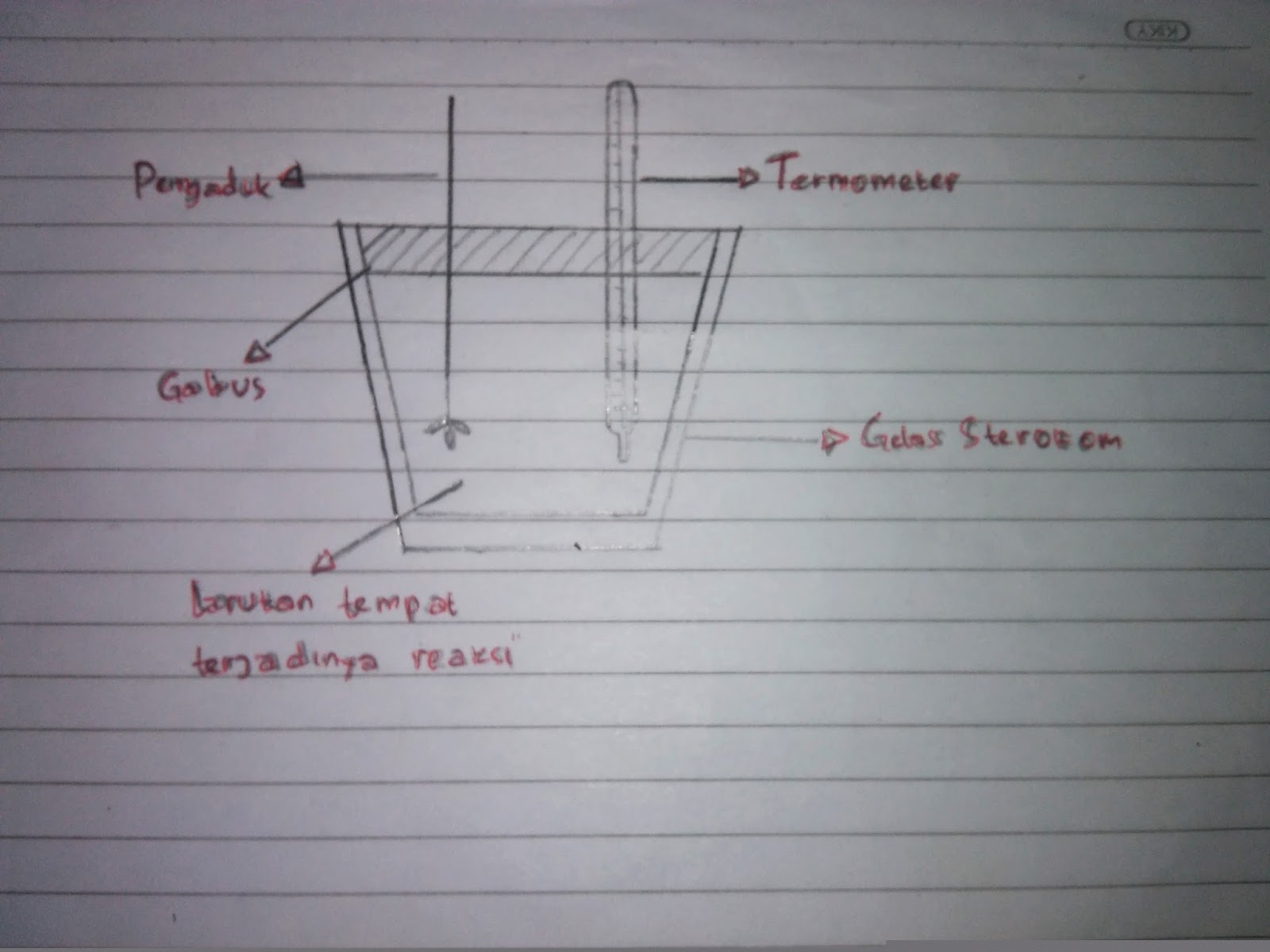
Pengertian Kalorimeter. Kalorimeter adalah alat untuk mengukur jumlah kalor yang terlibat pada suatu perubahan atau reaksi kimia. Proses dalam kalorimeter berlangsung secara adiabatik, yaitu tidak ada kalor yang keluar atau masuk dari kalorimeter. Kalorimetri adalah proses pengukuran jumlah kalor reaksi yang diserap atau dilepaskan pada suatu.
Lembar Kerja Praktikum SMA (Kalorimeter) RUMUS MATEMATIKA FISIKA
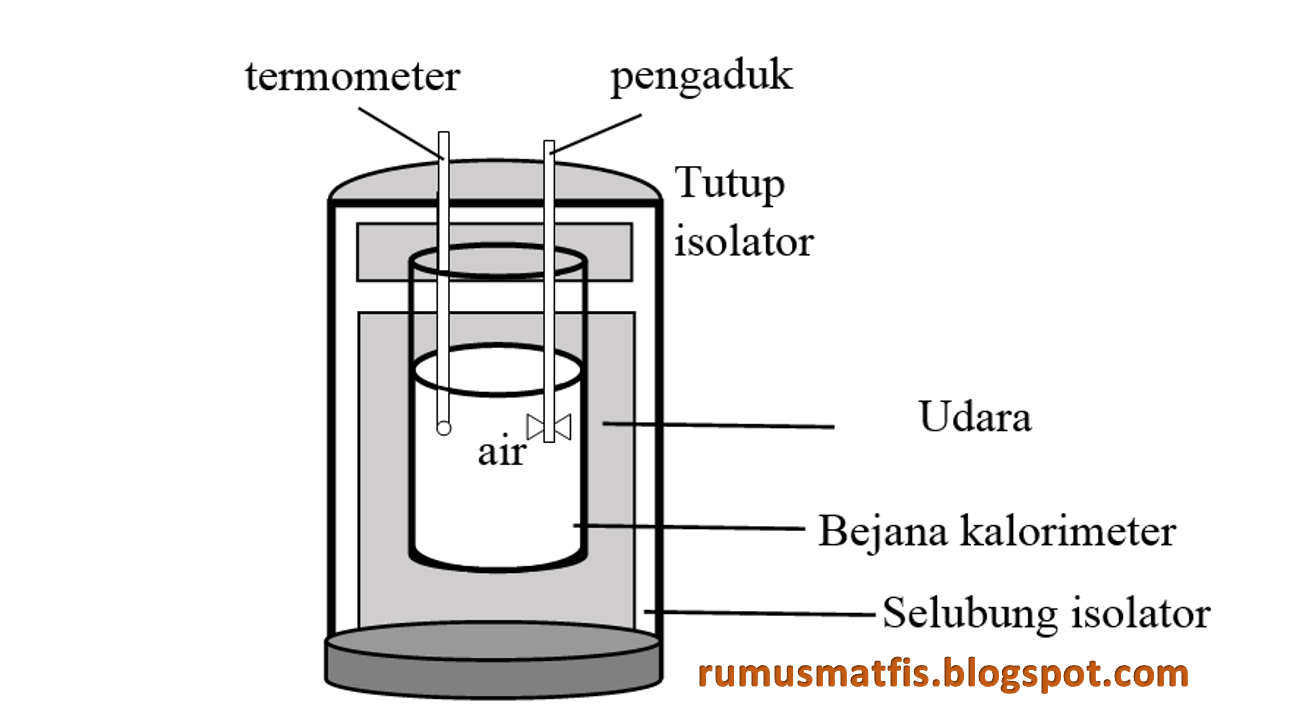
Penjelasan tentang kalorimeter masih jauh dari selesai jika kita tidak membahas bagaimana cara kerja dari alat ini. Untuk itu, kita akan membahasnya dalam 12 langkah yang mudah diikuti. Simaklah pembahasan berikut ini dengan baik, agar kamu dapat memahami bagaimana kalorimeter bekerja. Langkah-Langkah Langkah 1: Mengukur Massa Bahan Kimia
Calorimetry Pathways to Chemistry
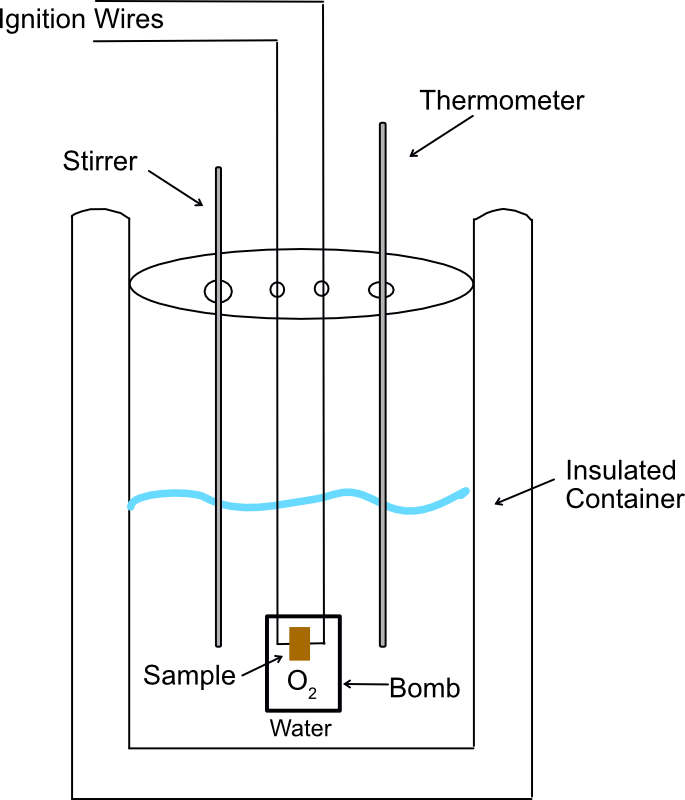
Tertarik tahu bagaimana cara kerja kalorimeter? Anda akan tercengang dengan keajaiban di balik alat yang cukup sederhana ini. Temukan jawabannya di sini, mulai dari prinsip dasarnya hingga proses pengukurannya yang akurat. Dapatkan penjelasan menarik tentang perlunya kalorimeter dalam berbagai bidang, seperti ilmu kimia, fisika, dan juga dalam dunia kuliner.
Penjelasan Mengenai Kalorimetri ( Termokimia Part Iv ) JUARA SATU
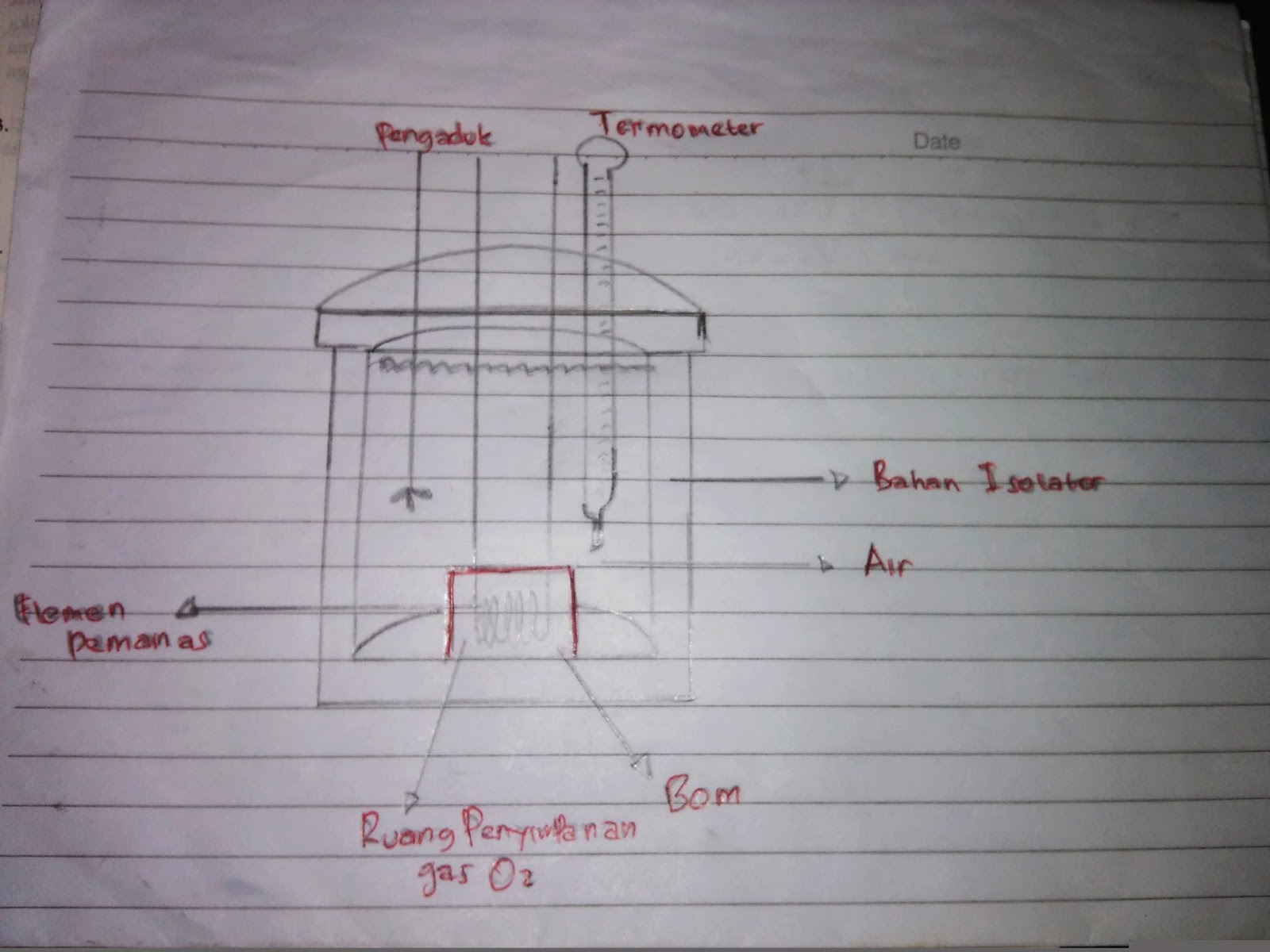
Kalorimeter adalah alat yang digunakan untuk mengukur jumlah panas yang terlibat dalam suatu reaksi kimia atau perubahan fisik. Alat ini umumnya terbuat dari dua bagian utama, yaitu bejana kalorimeter dan termometer. Cara kerja kalorimeter adalah dengan memanfaatkan prinsip kekekalan energi. Ketika suatu reaksi kimia atau perubahan fisik.

Kalorimeter bom
Awalnya, kalorimeter hanya terdiri dari dua wadah yang ditempatkan di dalam satu sama lain, dengan ruang hampa udara di antara keduanya. Namun, seiring berjalannya waktu, kalorimeter telah mengalami perkembangan yang signifikan dalam hal desain dan presisi pengukuran.. Bagaimana cara kerja kalorimeter? Kalorimeter bekerja dengan prinsip.

10.2 Calorimetry Chemistry Fundamentals
1. Kalorimeter adalah alat yang digunakan untuk mengukur jumlah energi termal yang dilepaskan dalam suatu reaksi kimia atau fisika. 2. Cara kerja kalorimeter terdiri dari tiga bagian utama yaitu mengukur jumlah energi yang dibutuhkan untuk mengubah suatu bahan dari satu bentuk ke bentuk lain, mengukur jumlah energi yang dilepaskan oleh reaksi.

Cara Melakukan Pengukuran Kalorimeter Bom YouTube
Di dalam ilmu kimia, kalorimeter adalah sebuah alat yang digunakan untuk mengukur jumlah energi panas yang terlibat dalam suatu reaksi kimia atau perubahan fisika. Alat ini penting dalam pemahaman tentang termokimia, yang adalah cabang ilmu kimia yang mempelajari tentang energi panas yang terkait dengan reaksi kimia dan perubahan fisika. Dalam artikel ini, kita akan membahas

Memahami Kalor dan RumusRumusnya Fisika Kelas 11
Kesimpulannya, prinsip kerja kalorimeter sangat beragam tergantung dari jenis kalorimeter yang digunakan. Namun, secuil prinsip yang mendasar adalah hukum kekekalan energi dan jumlah kalor yang diterima atau dilepaskan oleh sistem. Penggunaan kalorimeter sangat penting untuk memahami dan mengukur kalor dalam berbagai disiplin ilmu.

Analisa Kalori dengan Bom Kalorimeter
Cara kerja kalorimeter. Seperti yang Anda lihat di bagian sebelumnya, ada banyak jenis kalorimeter, sehingga cara kerjanya berbeda-beda. Berikut ini penjelasan penggunaan kalorimeter adiabatik, karena kalorimeter ini paling banyak digunakan dalam eksperimen laboratorium. Pengoperasian kalorimeter berhubungan dengan pengocokan shaker.
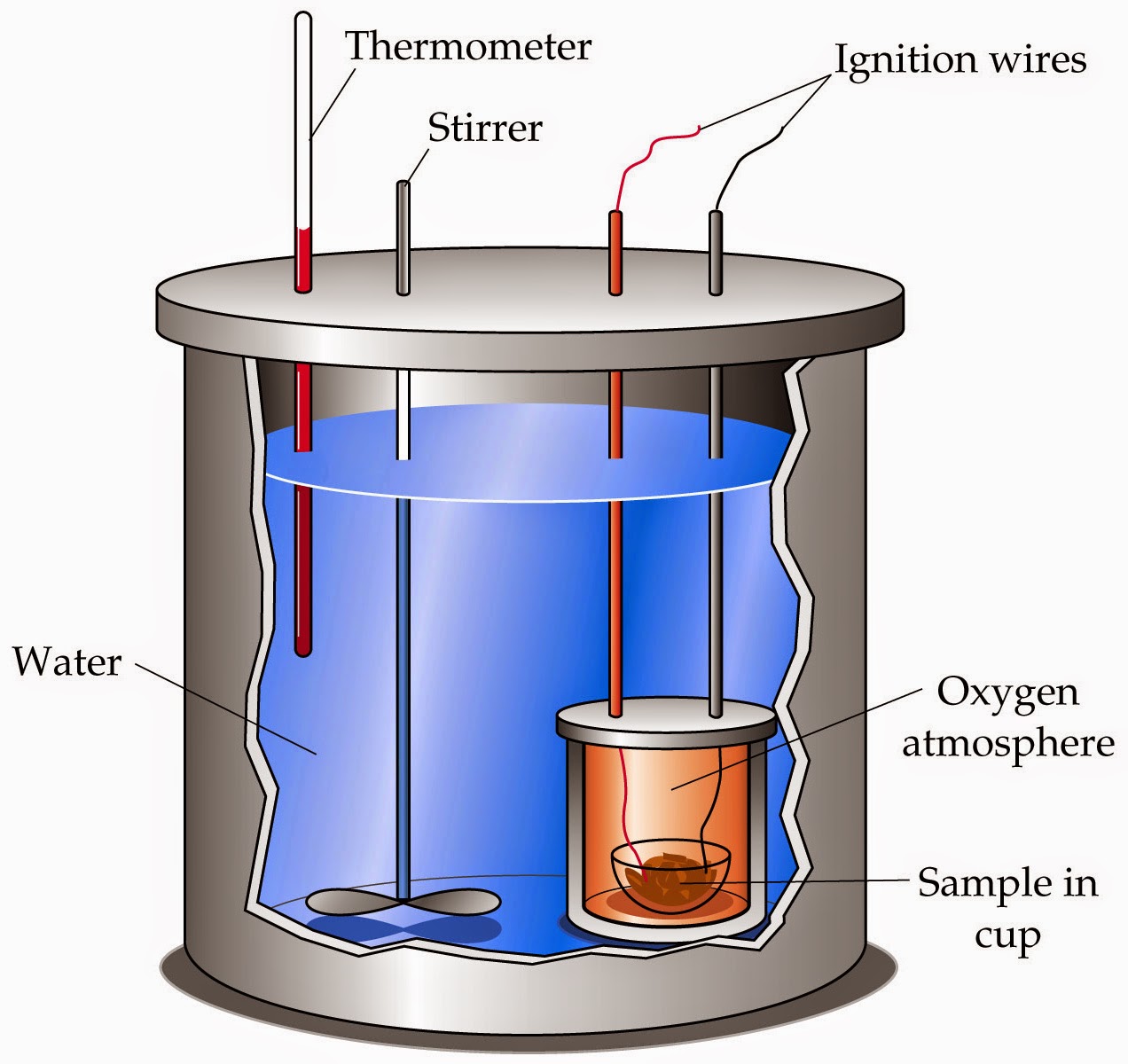
Termodinamika DimanaMana Prinsip Kerja Kalorimeter
19 Desember 2023 oleh Abdullah Ahmad. Prinsip Kerja Kalorimeter : Kalorimeter adalah alat yang digunakan untuk mengukur jumlah panas yang dikeluarkan atau diserap dalam suatu reaksi kimia atau perubahan fisika. Prinsip kerja kalorimeter didasarkan pada konsep transfer panas antara sistem yang diamati dan lingkungan sekitarnya.
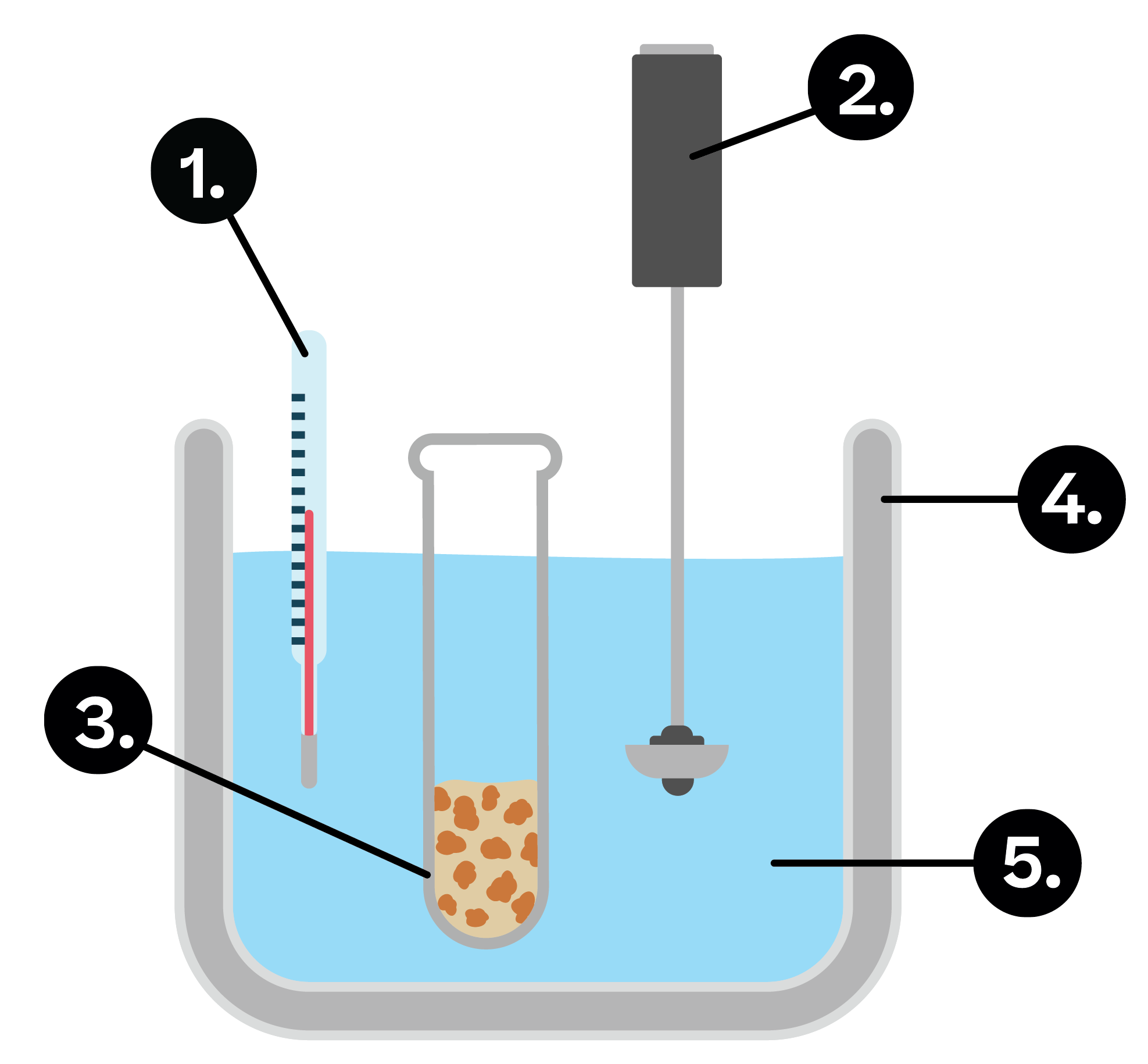
Kalorimetrie Chemie Erklärung & Übungen evulpo
Kalorimeter dapat membantu kita memahami seluk beluk alam, mengukur energi yang terkandung dalam sistem termodinamika. Mengukur dan memahami kalor dalam sistem termodinamika dapat memberi kita wawasan mengenai cara kerja materi, sifat-sifatnya, dan proses alam yang lebih luas. Dalam artikel ini, kita akan melihat cara kerja dari kalorimeter dan cara menggunakannya. Penjelasan dan Jawaban.
/cross-section-of-a-typical-bomb-calorimeter--141482586-5aa68ad4642dca00367be3f3.jpg)
คืออะไร Calorimeter?
3. Cara Kerja Kalorimeter 🕹️. Cara kerja kalorimeter sendiri tergantung pada jenis kalorimeter yang digunakan. Namun, prinsip dasarnya adalah dengan mengukur perubahan suhu yang terjadi pada benda saat panas ditambahkan atau diambil dari benda tersebut. Dari perubahan suhu yang terjadi, kita dapat menghitung jumlah panas yang ditransfer. 4.

Cara Kerja Kalorimeter Bom
Kalorimeter Adiabatik: Kalorimeter ini dirancang untuk mengisolasi sistem dari lingkungan sekitarnya, sehingga tidak ada pertukaran panas yang terjadi.. perbedaan antara kalorimeter bomb dan kalorimeter adiabatik, bagaimana cara kerja kalorimeter, apakah ada kalorimeter yang digunakan dalam penelitian biologi, dan apakah kalorimeter dapat.

[SANGAT MUDAH] Cara menghitung kalor reaksi pada kalorimeter (PART 2) YouTube
Cara Kera Kalorimeter Bom: Susun alat kalorimeter; Isi gelas kimia dengan 50 mL NaOH;. Setelah kristal LiOH itu larut, ternyata suhu kalorimeter beserta isinya naik dari 24°C menjadi 35°C. Kalor jenis larutan = 4,2 J/g°C dan kapasitas kalor kalorimeter = 12 J/°C. Tentukan besarnya entalpi pelarutan LiOH dalam air sesuai persamaan reaksi:

KALORIMETER Menghitung Perubahan Entalpi dengan Kalorimetri Kimia kelas XI YouTube
Pengukuran kalor jenis suatu benda, misalnya logam dilakukan dengan memasukkan logam panas ke dalam kalorimeter berisi air dingin. Ketika benda bercampur dengan air, suatu saat akan didapatkan suhu akhir campuran. Dengan menggunakan Asas Black, kita dapat menentukan kalor jenis suatu zat pada kalorimeter dengan menggunakan persamaan berikut.

Simpel Konsep Menentukan ∆H Reaksi Berdasarkan Eksperimen / Kalorimeter (Bagian I) YouTube
Kalorimeter adalah alat yang digunakan untuk mengukur perubahan suhu dari sejumlah zat (biasanya air) dari panas spesifik yang diketahui. Perubahan suhu ini disebabkan oleh kalor yang diserap atau dilepaskan dalam proses yang sedang diamati; kimia jika merupakan reaksi, atau fisika jika terdiri dari perubahan fase atau keadaan.