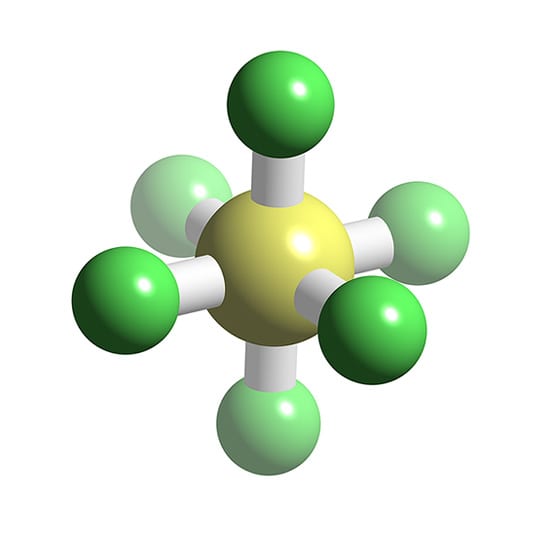
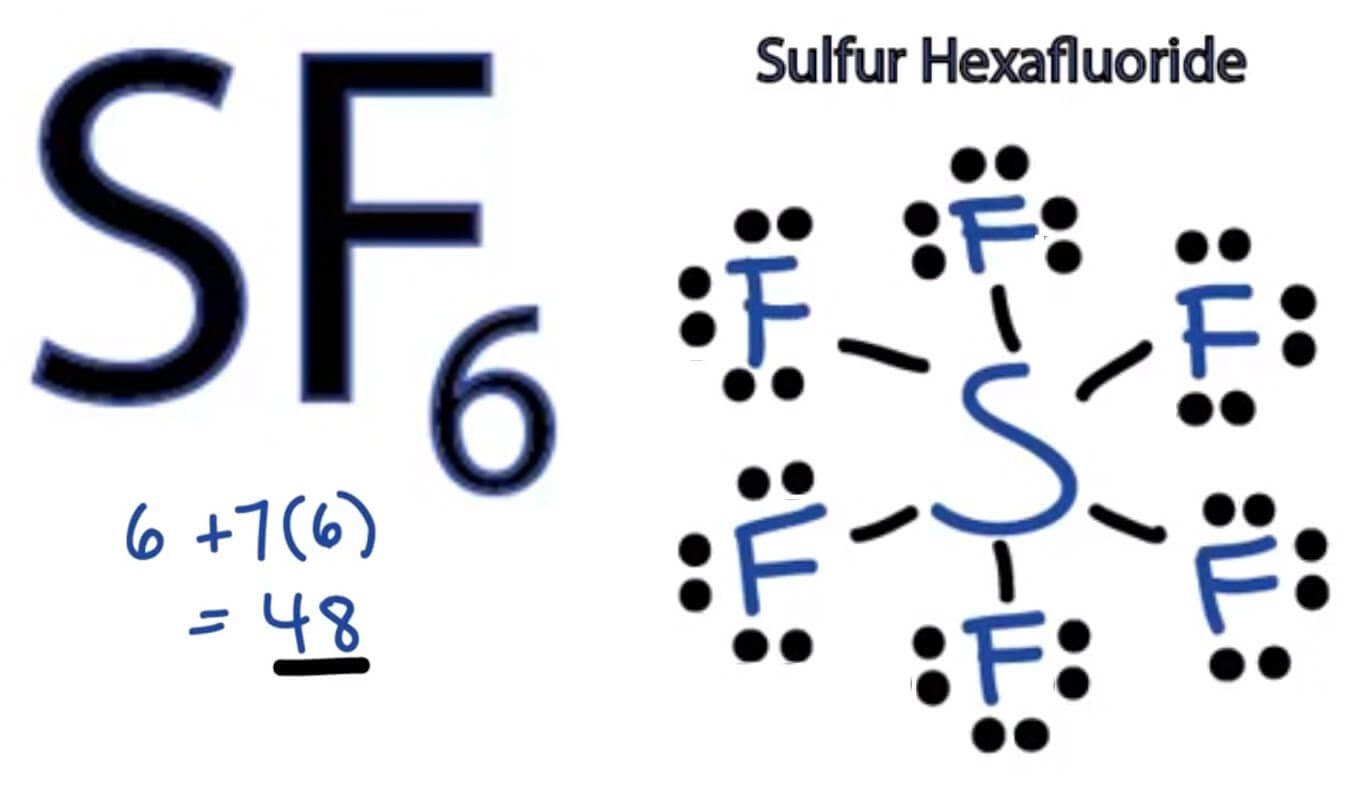
SF6 Sulfur hexafluoride
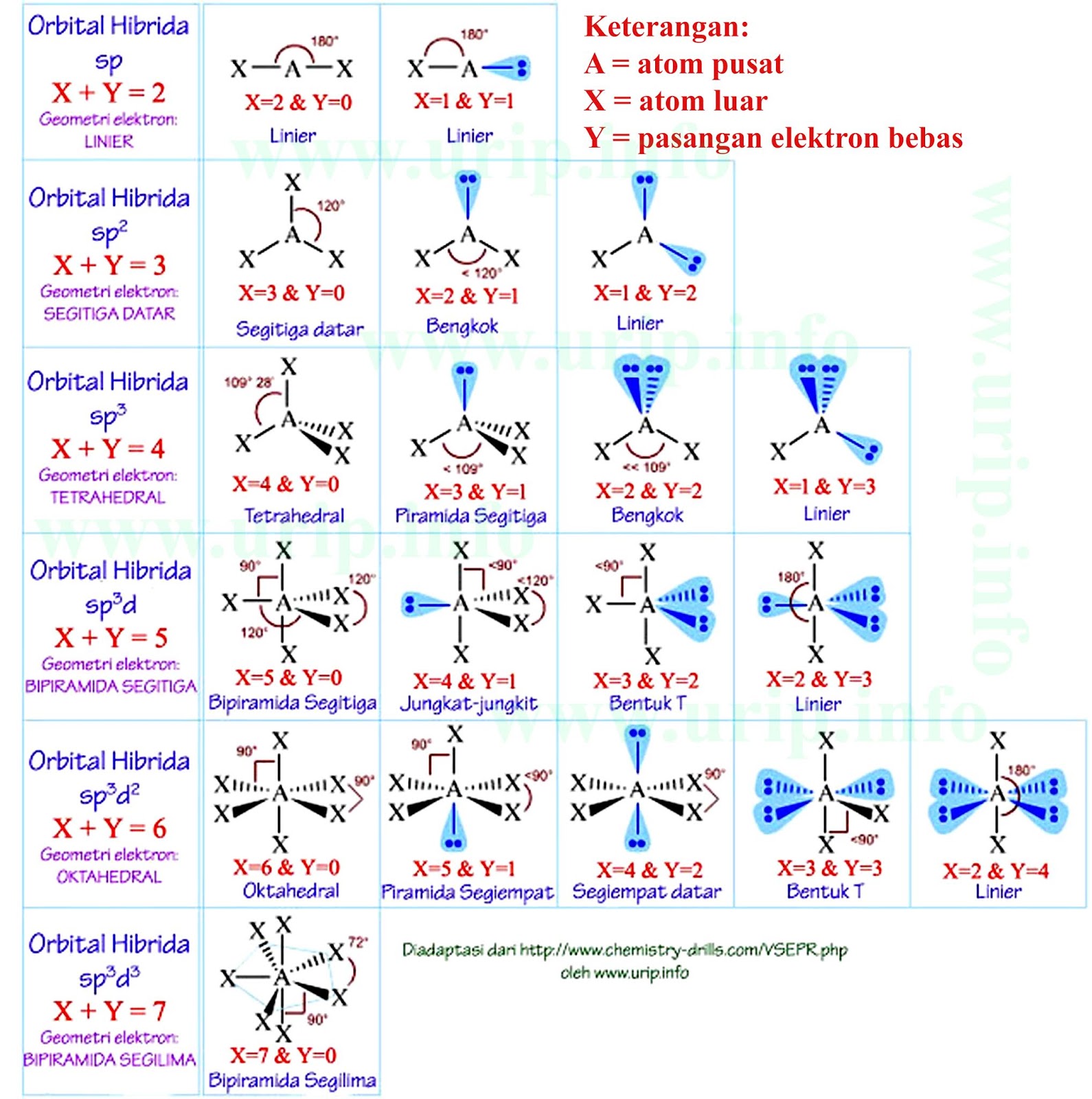
n: jumlah PEI dalam molekul. E: pasangan elektron bebas (PEB) m: jumlah PEB dalam molekul. Ada 11 bentuk molekul berdasarkan teori domain elektron, yaitu linear, segitiga planar, segiempat piramida, seesaw atau jungkat-jungkit, bentuk T, oktahedral, bentuk bengkok, tetrahedral, segitiga piramida, bentuk V, dan segitiga bipiramida.

Pasangan Gambar Yang Merupakan Molekul Senyawa Adalah denah
Teori Bentuk Molekul. 1. Teori VSEPR. Bunyi teori VSEPR adalah pasangan elektron dalam ikatan kimia ataupun pasangan elektron yang tidak dipakai bersama (yaitu pasangan elektron "mandiri") saling tolak-menolak, pasangan elektron cenderung untuk berjauhan satu sama lain.
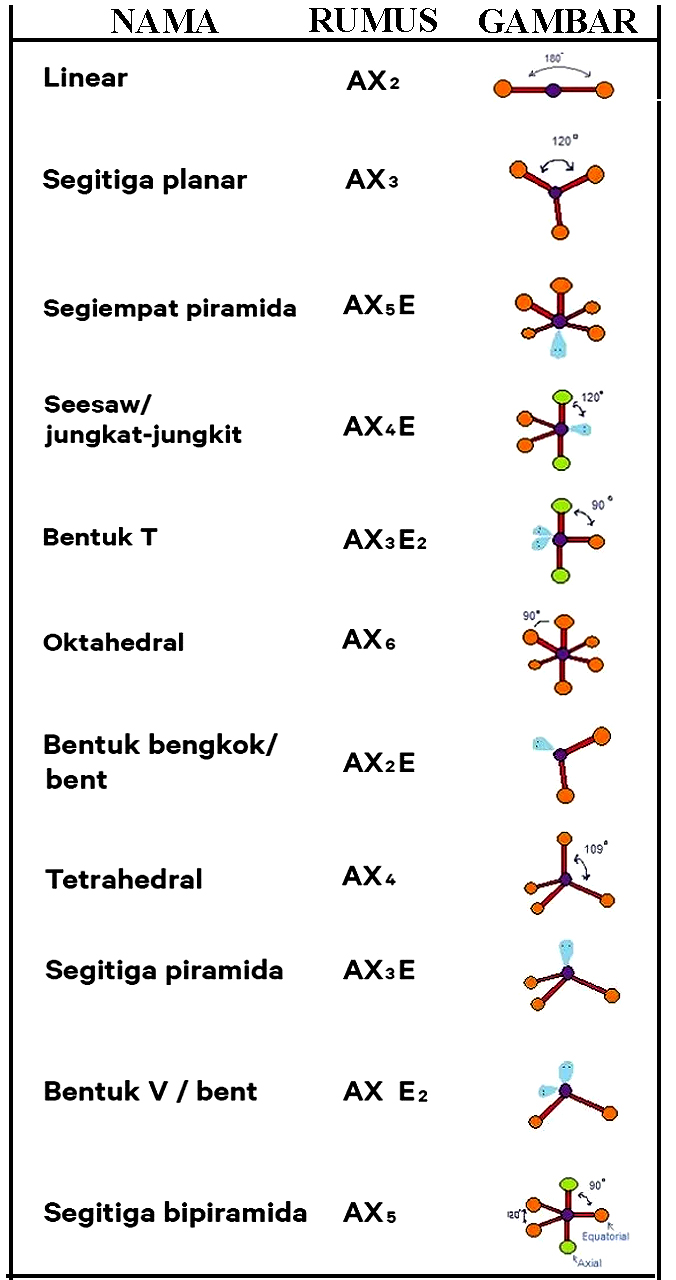
Bentuk Bentuk Molekul Menurut Teori Domain Elektron dan Hibridisasi Anto Tunggal
Sehingga tipe molekul adalah AX 2 E 2 (bentuk V) senyawa : konfigurasi atom pusat 15 P = 2, 8, 5 . PEI = 5. Sehingga tipe molekul adalah AX 5 (bipiramida trigonal) Jadi, senyawa 1 = oktahedral, senyawa 2 = tetrahedral, senyawa 3 = bentuk V, senyawa 4 = bipiramida trigonal.
Sf6 lewis structure
S {-6+6} + 6 (F {-1+1}) ⇒ SF 6. Hibridisasi Atom S, Bentuk Molekul, dan Kepolaran SF2. Detil yang khusus membahas tentang hibridisasi, bentuk molekul, dan kepolaran senyawa silakan disimak di sini. Bentuk dasar (geometri elektron, semua pasangan elektron diperhatikan) SF 2 adalah tetrahedral. Bentuk molekul (geometri molekul, hanya.
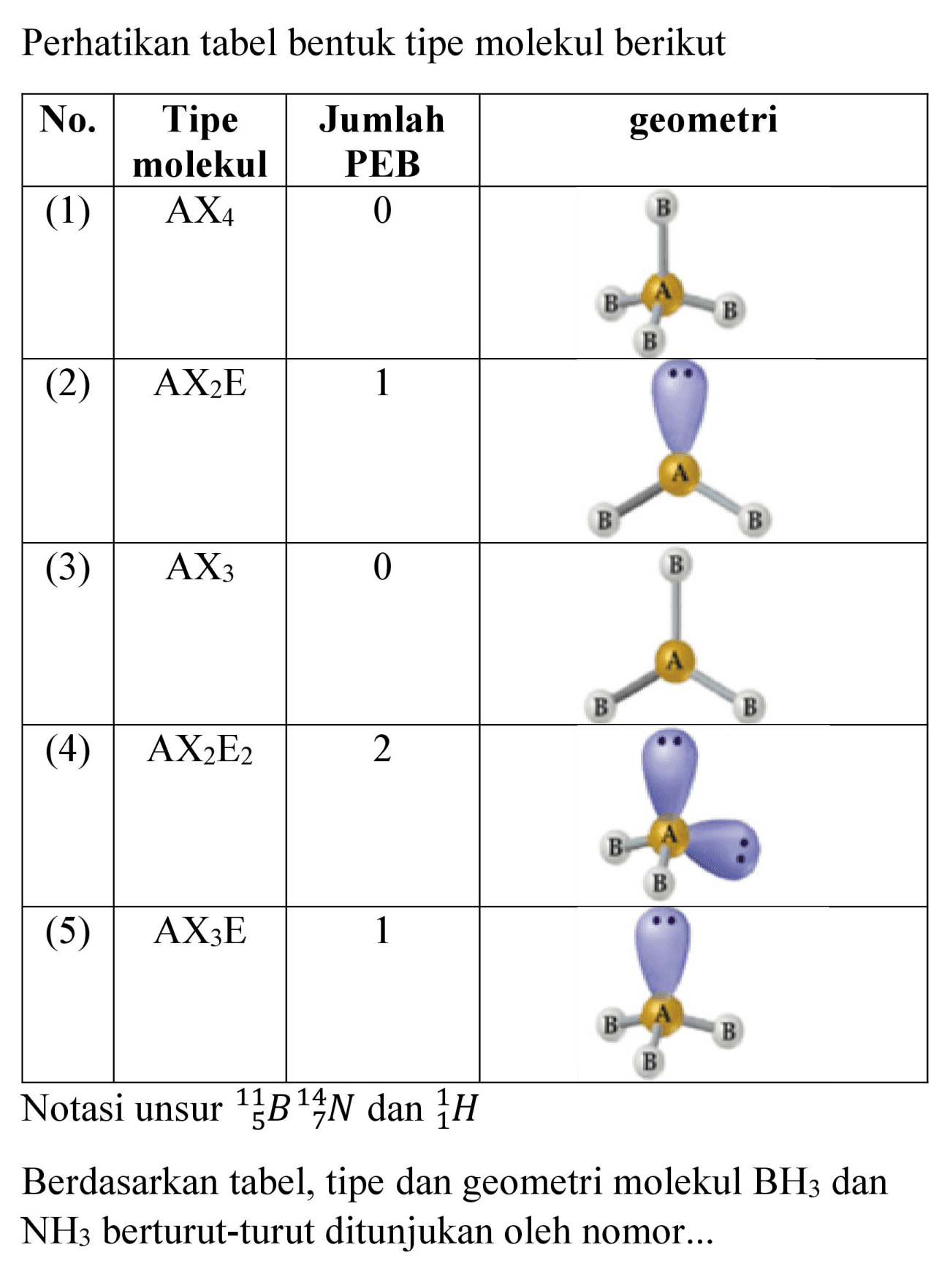
Ramalkan bentuk molekulmolekul di bawah ini dengan mengg...
Pengertian geometri molekul adalah susunan ruang atom-atom dalam molekul. Pengertian hibridisasi adalah suatu konsep bersatunya orbital-orbital atom membentuk orbital hibrid yang baru dalam pembentukan ikatan. Konsep ini berfungsi menjelaskan terjadinya bentuk/geometri molekul. Teori VSEPR (Valence Shell Electron Pair Repulsion)

SF6 Lewis Structure, Molecular Geometry, Hybridization, and MO Diagram Techiescientist
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Bentuk molekul SF6 adala.
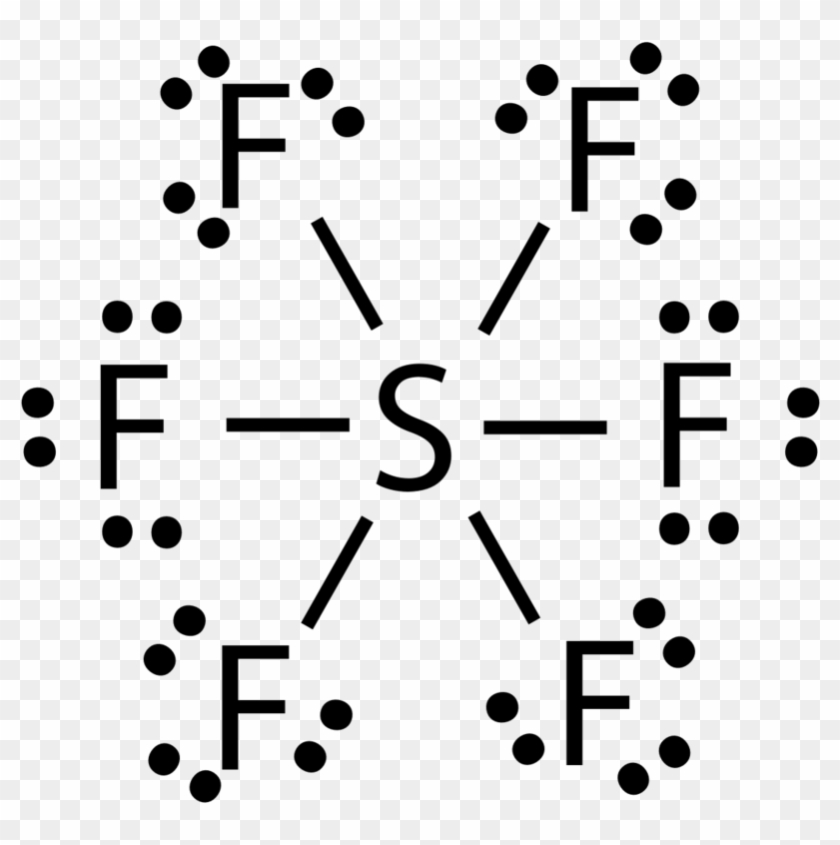
Drawn Molecule Sf6 Sf6 Lewis Dot Structure Free Transparent PNG Clipart Images Download
H C + 4 H H C H H f GEOMETRI/BENTUK MOLEKUL Bentuk molekul ditentukan melalui percobaan, namun demikian dapat pula diramalkan berdasarkan pemahaman struktur elektron dalam molekul itu. Teori Domain Elektron Domain elektron berarti kedudukan elektron atau daerah keberadaan elektron disekitar atom pusat. Jumlah domain elektron ditentukan sbb: 1.
bentuk Orbital hibrida SF6...
Belerang heksafluorida (SF 6) adalah suatu gas anorganik yang tidak berwarna, tidak berbau, tidak mudah terbakar, dan sangat berpotensi merupakan gas rumah kaca, yang mana ia merupakan insulator listrik yang baik. [4] SF6 memiliki geometri molekul oktahedral, terdiri dari enam atom fluor yang menempel pada atom pusat belerang.
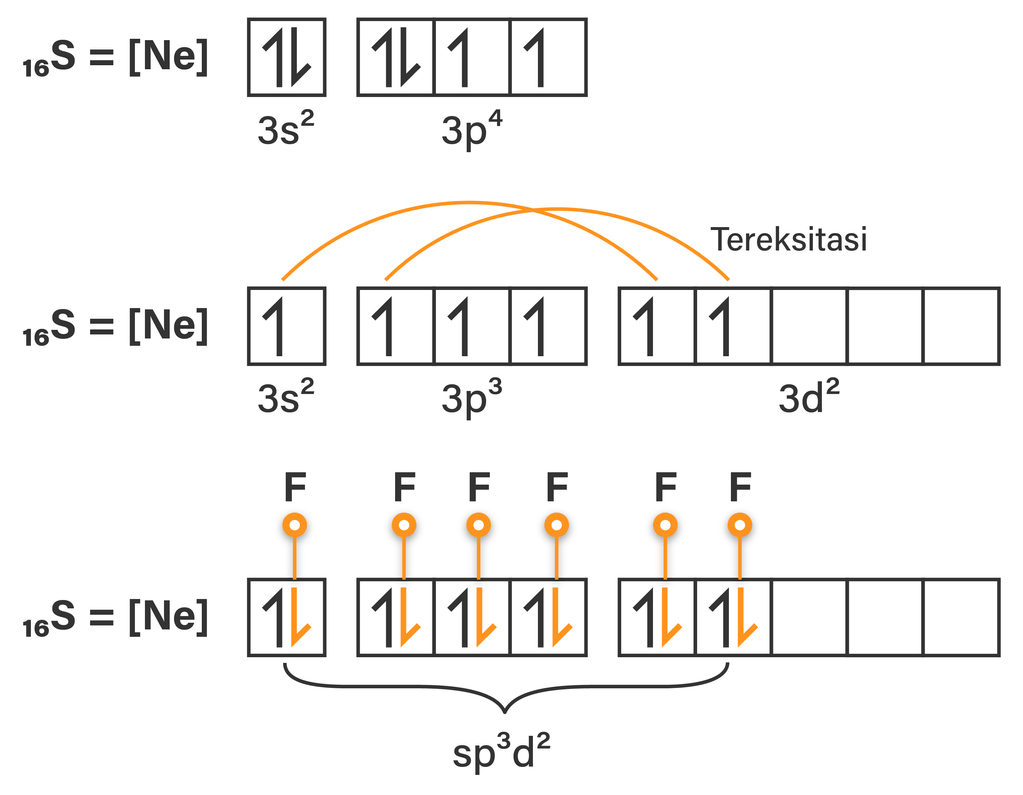
jelaskan proses hibridisasi molekul SF6...
Langkah 1: Temukan jumlah total elektron valensi dalam molekul SF6. Untuk mengetahui jumlah total elektron valensi dalam molekul SF6 (sulfur heksafluorida), pertama-tama Anda perlu mengetahui elektron valensi yang ada dalam atom belerang dan juga atom fluor. (Elektron valensi adalah elektron yang ada di orbit terluar atom mana pun.)

Ikatan Kimia Kelas 10 • Part 13 Tipe Molekul, Bentuk Molekul, Hibridisasi, dan Kepolaran IF3
Pada terdapat 1 atom S dan 6 atom F. Langkah penentuan bentuk molekul adalah sebagai berikut.. Menentukan elektron valensi dengan 6 elektron valensi dengan 7 elektron valensi; Menentukan bentuk mokelul Senyawa memiliki 6 buah pasang elektron ikatan dan tidak memiliki pasangan elektron bebas, sehingga bentuk geometri molekulnya adalah oktahedron.; Jadi, jawaban yang tepat adalah E.

The skeleton of SF6 molecules. The vector potentials of the twocolor Download Scientific Diagram
Video ini berisi materi Ikatan Kimia kelas 10, dan di part yang ketigabelas ini masih membahas bagaimana cara menentukan bentuk molekul suatu senyawa dengan.
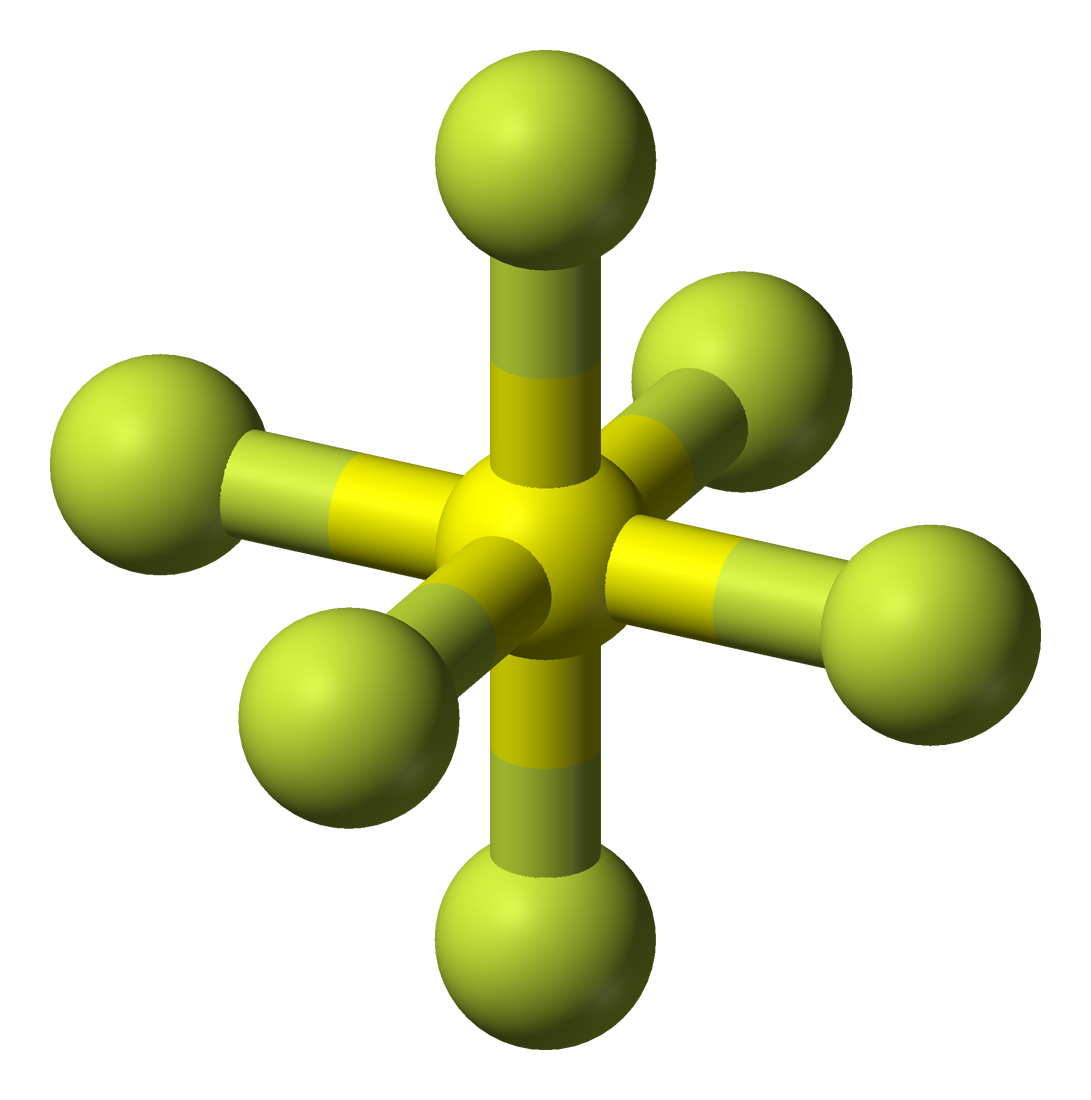
Bentuk Molekul SF6 MateriKimia
SF6. 2. Menentukan hibridisasi dengan cara SUPER "Solusi Quipper" a. BeCl2. b. SF6. Contoh soal 1. Contoh soal 2. Bentuk Molekul. Bentuk molekul adalah susunan atom-atom di dalam molekul dalam bentuk tiga dimensi. Siapa sangka jika bentuk molekul inilah yang menyebabkan perbedaan sifat fisis dan kimia suatu senyawa, misalnya titik leleh.
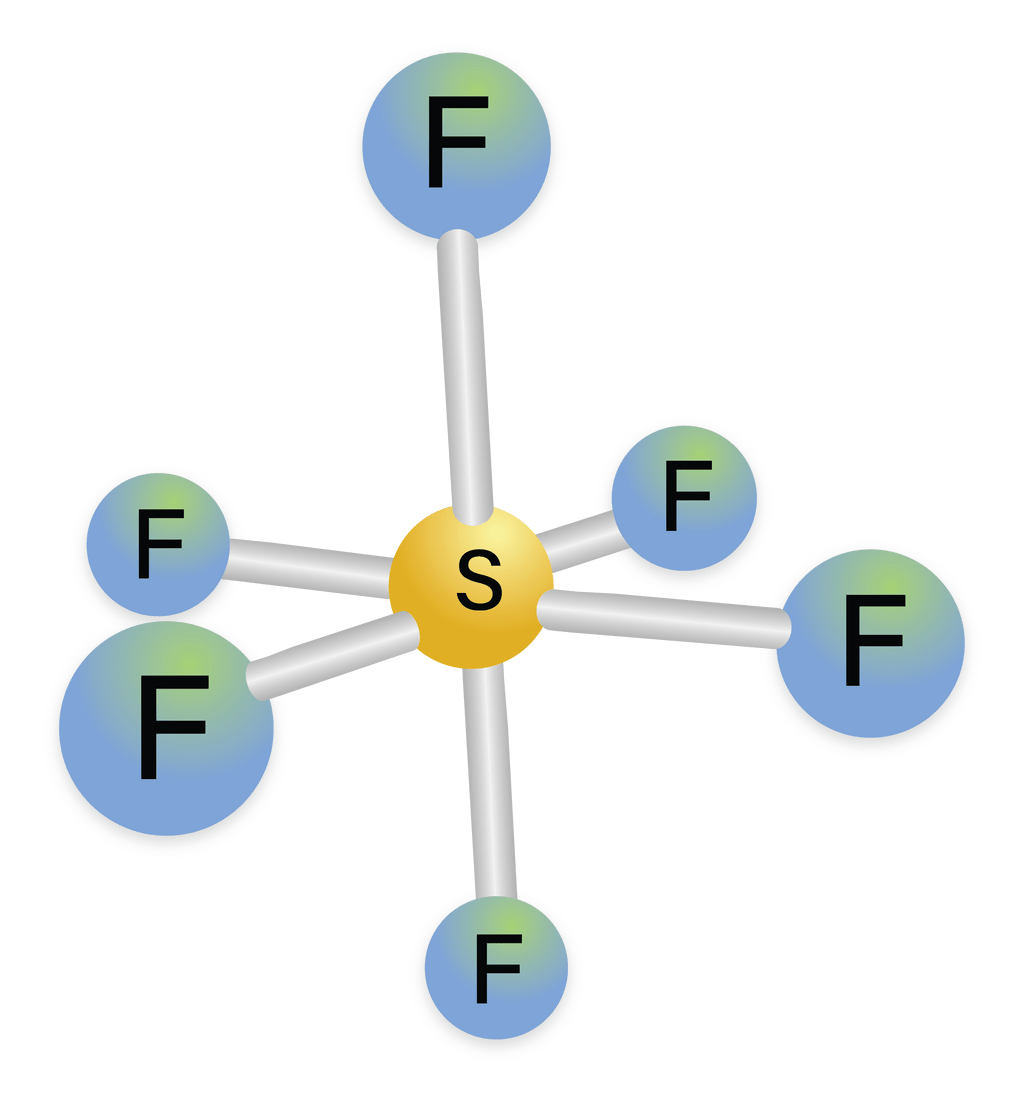
Tentukan jumlah pasangan elektron terikat, jumlah
Molekul ini umumnya nonpolar karena bentuknya yang sangat simetris. Sudut ikatan dalam bentuk molekul octahedral terdiri dari sudut-sudut tertentu yang tetap. Contoh umum dari molekul dengan bentuk octahedral adalah sulfur heksafluorida (SF6). Dalam molekul SF6, terdapat satu atom sulfur (S) yang terikat secara kovalen dengan enam atom fluor (F).

BENTUK MOLEKUL SENYAWA VSEPR dan HIBRIDISASI YouTube
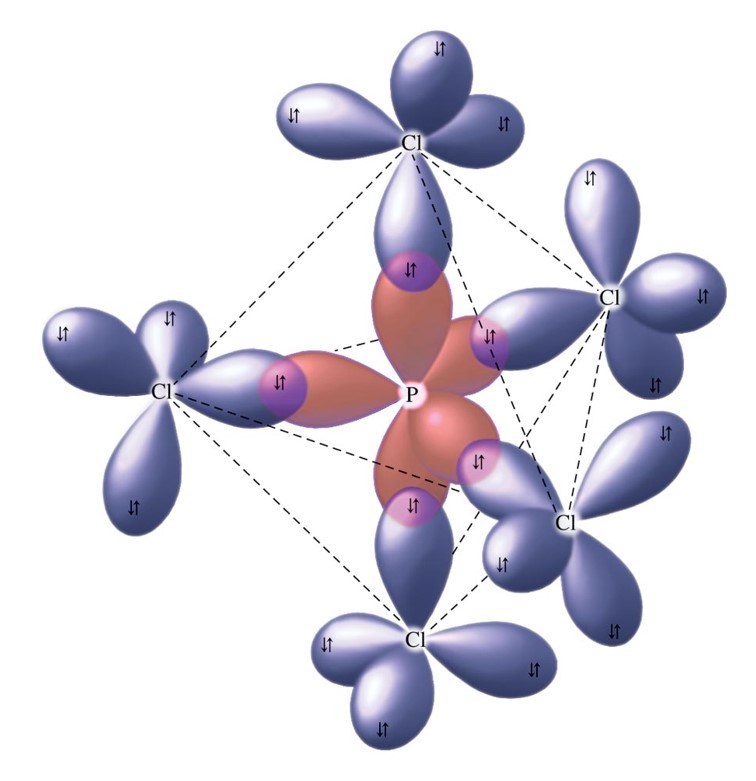
Sedangkan PEB dapat ditentukan dengan rumus yaitu: Maka memilikiPEI = 4, dan atom pusat S merupakan golongan VIA artinya ev = 6, maka: Dengan demikian maka jumlah domain elektron adalah 5(4 PEI+1 PEB), sehingga bentuk dasar senyawanya adalah segitiga bipiramida. karena ada nya PEB maka bentuk molekul nya akan berubah menjadi: Dengan demikian.
SF6分子幾何学、ルイス構造、形状、および極性 Peaceful Place
Rumus notasi VSEPR. Notasi VSEPR menentukan bentuk molekul melalui rumus umum yang memperhitungkan jumlah pasangan elektron pada atom. Berikut adalah rumus notasi VSEPR: A: atom pusat. X: Elektron terikat. a: jumlah pasangan elektron ikatan (PEI) yang terikat pada atom pusat. E: kelompok elektron valensi non-ikatan (PEB)
Cara Paling Mudah Menentukan Bentuk Molekul Ion Poliatomik Serba Ada
Bentuk molekul CH4 adalah tetrahedral, sama seperti struktur orbital hibrida sp3 (lihat Gambar 2.15).. Contoh molekul dengan bentuk trigonal bipiramidal adalah PCl5 dan contoh molekul oktahedral adalah SF6 . Tinjau molekul PCl5 dengan atom P sebagai atom pusat. Konfigurasi elektronnya: 15P: 1s2 2s2 2p6 3s2 3p3 3d0 . Hibridisasi satu orbital.