
LARUTAN ELEKTROLIT DAN NONELEKTROLIT ( KIMIA SMA KELAS 10 ) YouTube
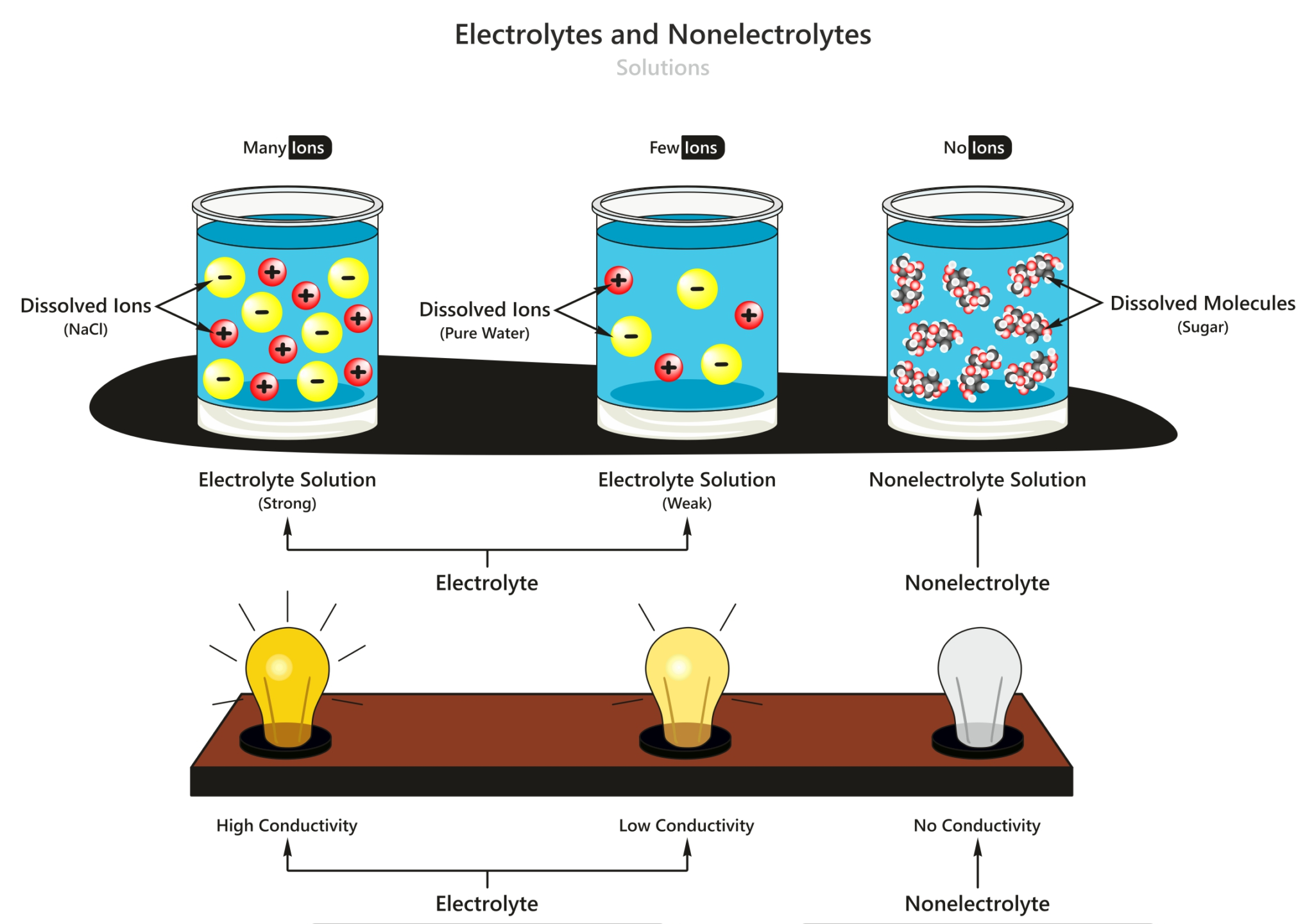
Larutan Non-Elektrolit. Larutan Non-elektrolit adalah larutan yang tidak dapat membentuk ion-ion dalam pelarutnya sehingga tidak dapat menghantarkan listrik. Ciri dari larutan ini ketika dilakukan percobaan adalah tidak dapat menyalakan lampu dan tidak menghasilkan gas pada kedua elektrodenya.
Mengenal Pengertian Larutan Elektrolit Dan Non Elektrolit Sifat Ciri Unamed
Pengertian larutan non elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik. Larutan non elektrolit tidak dapat menghantarkan arus listrik karena senyawa nonelektrolit tidak dapat terionisasi sehingga ion-ion penyusunnya tidak dapat bergerak bebas. Contoh larutan nonelektrolit: Urea, glukosa, sukrosa, benzena, dan CCl 4.
Ciri Ciri Amp Perbedaan Larutan Elektrolit Dan Non Elektrolit Contoh Riset
NaCl (s) → Na+ (aq) + Cl− (aq) Perlu elo ingat bahwa larutan elektrolit kuat selalu terdiri dari asam kuat, basa kuat dan garam. Nah, larutan NaCl (garam) bukan satu-satunya yang tergolong ke dalam larutan elektrolit kuat. Karena terdapat beberapa larutan yang dapat menghantarkan arus listrik adalah NaOH (soda api), H2SO4 (asam sulfat), HCl.

Larutan Elektrolit dan Non Elektrolit (Komponen Larutan)
Contoh larutan non elektrolit antara lain: Larutan urea (CON2H4 atau (NH2)2CO), Larutan sukrosa (C12H22O11) Larutan glukosa (C6H12O6), Larutan alkohol (C2H5OH, CH3OH, dan lainnya) Ciri-Ciri Larutan Non Elektrolit. Berikut ini adalah ciri-ciri Larutan non elektrolit: Tidak dapat terionisasi. Tidak dapat menghantarkan arus listrik atau isolator.

Mengenal Larutan Elektrolit dan Non Elektrolit Kimia Kelas 10
Konsep larutan elektrolit dan non-elektrolit pertama kali dijelaskan oleh ahli kimia asal Swedia, Svante August Arrhenius, pada tahun 1884. Menurut Arrhenius yang dikutip dari Kimia Dasar II oleh Elvy Rahmi Mawarnis, senyawa elektrolit dalam air akan terurai menjadi partikel-partikel yang berupa atom atau gugus atom bermuatan listrik yang.

Larutan Elektrolit dan Reaksi Redoks Kelas 10 • Part 1 Larutan Elektrolit dan Nonelektrolit
Contoh Larutan Elektrolit dan Larutan Non Elektrolit. Contoh larutan elektrolit. Larutan elektrolit kuat, contohnya: Asam kuat : HCI, HBr,. Ciri-Ciri dan Proses Pembentukan Tulang Rawan [TERLENGKAP] Sistem Saraf Pada Hewan (Vertebrata dan Avertebrata) dengan Penjelasan dan Contohnya TERLENGKAP;
Pengertian Larutan Elektrolit Non Elektrolit Ciri Ciri Dan Contohnya Riset
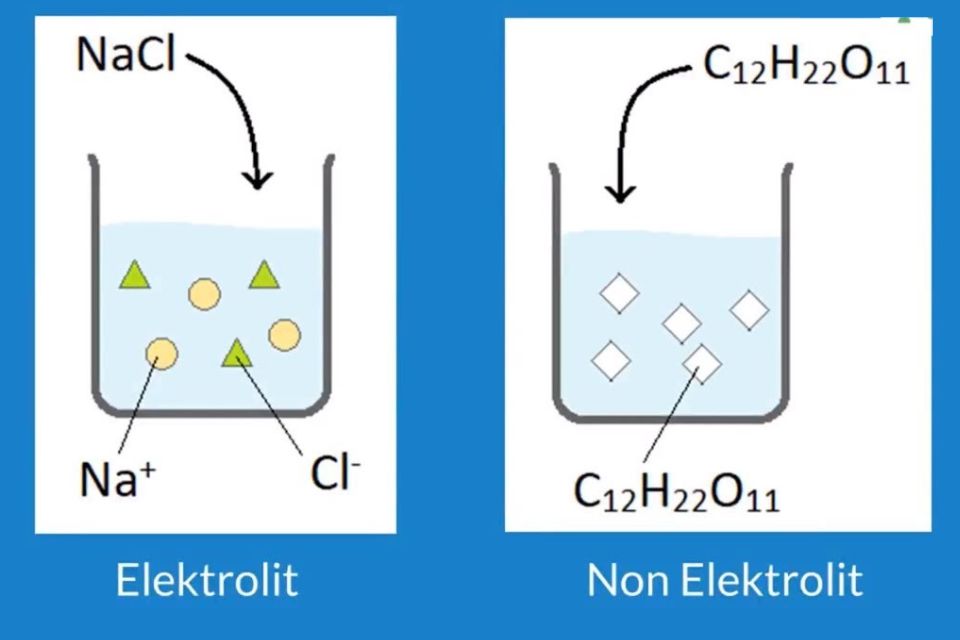
Pada larutan non elektrolit, zat non elektrolit yang terlarut tidak dapat terurai menjadi ion-ion, sehingga tidak terdapat ion-ion bebas yang dapat menghantarkan arus listrik. Sebagai contoh, larutan gula sukrosa (C 12 H 22 O 11 ) merupakan larutan non elektrolit.
Pengertian Ciri Ciri Dan Contoh Larutan Elektrolit Dan Non Elektrolit Riset Riset
Tidak terionisasi. Ciri-ciri larutan non elektrolit adalah tidak terionisasi ketika dilarutkan dalam air. Hal tersebut karena senyawa non elektrolit tidak memiliki ikatan ionic yang dapat putus ketika bereaksi dengan air. Dilansir dari Thought Co, senyawa non elektrolit cenderung memiliki ikatan kovalen dan merupakan nolekul non polar.
Mengidentifikasi Ciri Ciri Dan Perbedaan Larutan Elektrolit Dan Non Riset
Ciri-Ciri Larutan Elektrolit Kuat Terionisasi sempurna Derajat ionisasi sama dengan satu (α= 1) Dapat menghantarkan listrik Daya hantar listriknya kuat Memiliki banyak gelembung Lampu menyala terang Ciri-Ciri Larutan Elektrolit Lemah Terionisasi tidak sempurna/sebagian Derajat ionisasi kurang. Ciri-Ciri Larutan Elektrolit dan Non Elektrolit.

Elektrolit Kuat dan Elektrolit Lemah (Kimia SBMPTN, UN, SMA) YouTube
Seperti namanya, larutan non-elektrolit adalah larutan yang tidak dapat menghantarkan arus listrik. Jika disekitar penghantar listrik (electrode) tidak muncul gelembung-gelembung gas, dan lampu tidak menyala ketika diuji. Ciri-ciri dari larutan non-elektrolit: Pada larutan non elektrolit, senyawa dalam air tidak mengalami proses ionisasi.

Larutan Elektrolit dan Non Elektrolit (Kompone
Perbedaan larutan elektrolit dan non elektrolit memang dapat dilihat dari berbagai macam hal. Untuk larutan sendiri, tentu saja bukan kata yang asing untuk sebagian orang. Jika dilihat dari kaca ilmu bidang kimia, maka larutan sendiri merupakan campuran homogen antara dua zat atau lebih. Di dalam ulasan kali ini akan dibahas mengenai perbedaan.

30 Contoh Larutan Elektrolit dan Non Elektrolit
Larutan non elektrolit. Kebalikan dari larutan elektrolit adalah larutan non elektrolit, larutan ini tidak dapat menghantarkan arus listrik karena senyawa yang terdapat dalam larutan non elektrolit tidak dapat terionisasi menjadi ion-ion sehingga pada saat dilakukan percobaan, muncul ciri-ciri, seperti lampu tidak dapat menyala dan tidak menghasilkan gelembung gas di sekitar elektroda.

PPT LARUTAN ELEKTROLIT DAN NON ELEKTROLIT PowerPoint Presentation, free download ID4715206
Larutan elektrolit tinggi memiliki derajat ionisasi (α) yang mendekati 1, berarti zat terlarut hampi semuanya terionisasi. Adapun larutan elektrolit lemah memiliki derajat ionisasi jauh dibawah 1, berarti zat terlarut yang berubah menjadi ion hanya sedikit. Hal ini menyebabkan larutan elektrolit lemah menghantarkan listrik dengan kurang baik.

Mengenal Pengertian Larutan Elektrolit Dan Non Elektrolit Sifat Ciri Unamed
Berikut ini sifat dan ciri-ciri dari larutan non elektrolit: Tak memiliki kemampuan menghantarkan energi listrik. Lampu pada percobaan tidak akan menyala. Tidak ada proses ionisasi pada larutan. Tidak adanya gelembung gas. Itulah sifat dan ciri-ciri dari larutan non elektrolit. Contoh larutan ini misalnya adalah C2H 5 OH, CO(HN2) 2, CH 3 OH.

Materi Kimia Elektrolit dan Non Elektrolit YouTube
Sifat dari elektrolit biasa dimanfaatkan dalam proses elektrolisis untuk mendapatkan unsur atau campuran tertentu pada sebuah larutan. Pengertian dan Ciri-Ciri Larutan Elektrolit dan Nonelektrolit. Konsep larutan elektrolit dan nonelektrolit pertama kali dijelaskan oleh ahli kimia asal Swedia, Svante August Arrhenius, pada tahun 1884.

Larutan elektrolit dan non elektrolit
Artinya, larutan non elektrolit tidak mengandung ion-ion (kation atau anion) yang dapat menghantarkan muatan listrik. Dilansir dari Chemistry LibreTexts, hal tersebut karena zat non elektrolit tidak berdisosiasi sama sekali dan rumus kimia zat tersebut tidak berubah selama proses pelarutan. Zat elektrolit cenderung memiliki ikatan kovalen yang.