
Tentukan jumlah partikel (atom atau molekul) yang terdapat dalam a. 2 mol NH3 b. 1 mol Ca YouTube
3. Volume Molar (Vm) Volume molar menyatakan keadaan volume suatu gas dalam keadaan tertentu. Nilai volume molar terbagi menjadi 2 keadaan, yaitu: STP (Standard Temperature and Pressure). Keadaan ini disebut juga dengan keadaan standard berada pada suhu 0 0 C dan tekanan 1 atm. Nilai volume molar = 22,4 L/mol.
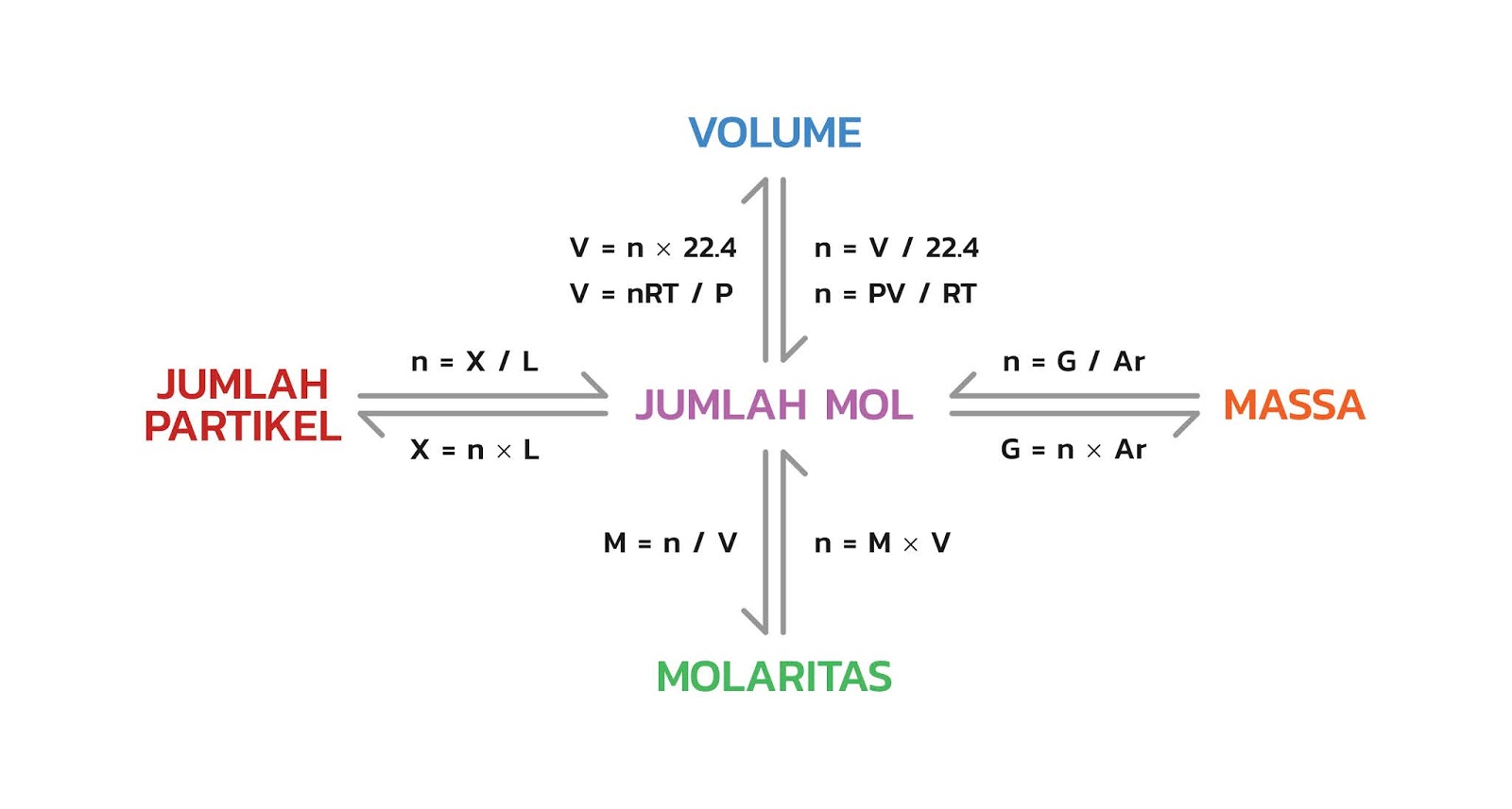
Hubungan Mol Dengan Jumlah Partikel Massa Volume Dan Molaritas Riset
Hubungan Mol dengan Jumlah Partikel Seperti yang udah kalian tahu nih, 1 mol menyatakan banyaknya partikel dalam suatu zat, yang mana jumlahnya sama dengan jumlah partikel dalam 12 g atom C-12. Berdasarkan penelitian pak Avogadro diketahui nih kalau dalam 1 mol atau 12 g atom C-12 terkandung 6,02 x 10²³ partikel.

Kumpulan Contoh Soal Konsep Mol dan Hubungannya dengan Jumlah Partikel, Massa Molar, dan Volume
Contoh soal hubungan mol dengan jumlah partikel, massa, dan volume zat kimia dapat digunakan untuk belajar. Pada pelajaran kimia, siswa dan siswi akan dihadapkan dengan berbagai materi. Salah satu materi yang akan dibahas adalah tentang hubungan mol dengan jumlah partikel. Materi ini cukup sulit, tetapi sangat penting untuk mengetahui reaksi kimia.
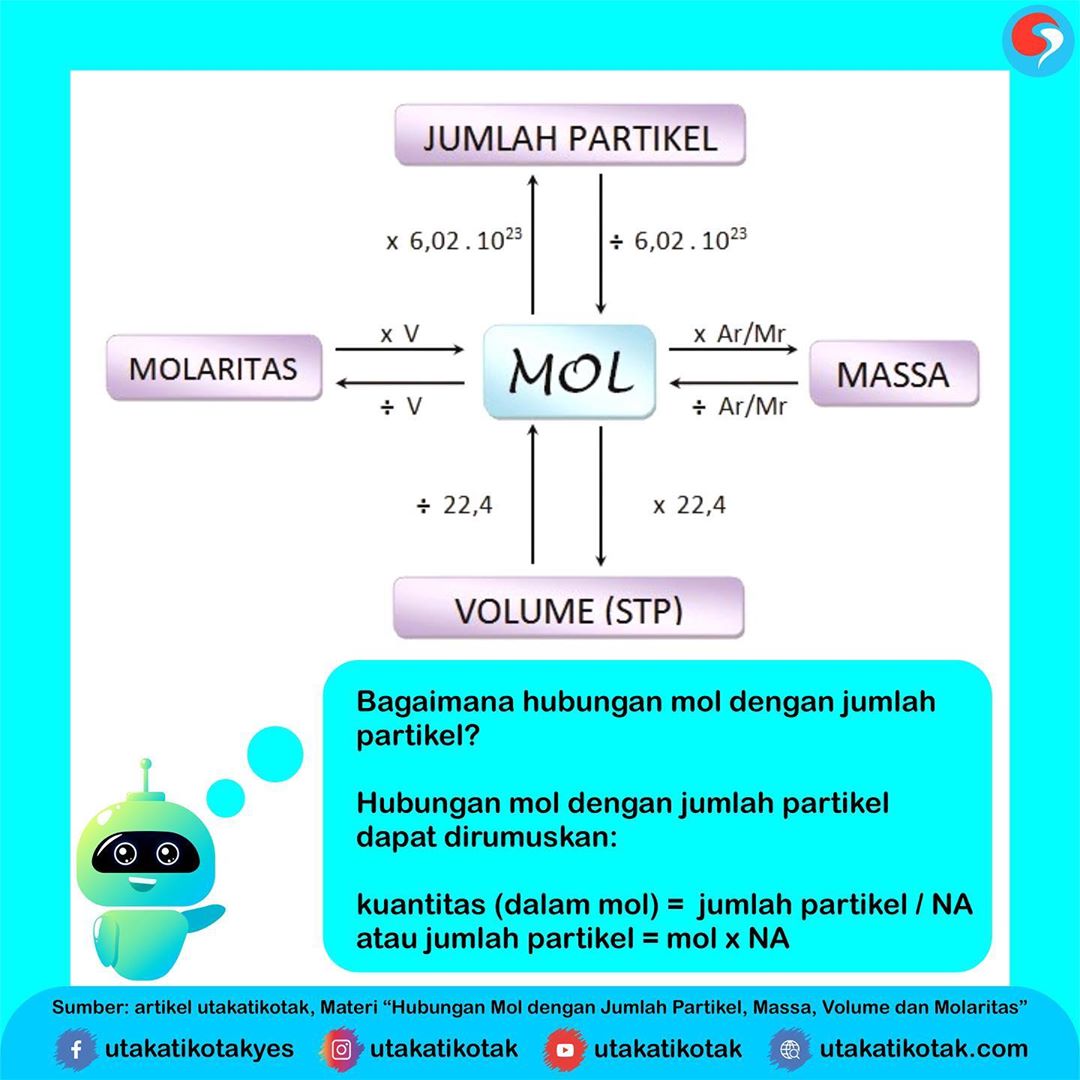
Hubungan Mol dengan Jumlah Partikel, Massa, Vo
Jumlah partikel H2O = Jumlah mol H2O x Bilangan Avogadro Jumlah partikel H2O = 0,5 mol x 6,022 x 10^23 partikel/mol Jumlah partikel H2O = 3,011 x 10^23 partikel Jadi, jumlah partikel H2O dalam 0,5 mol H2O adalah 3,011 x 10^23 partikel.. Contoh Soal ke-11: Soal selanjutnya akan menguji pemahaman kita tentang hubungan mol dengan jumlah partikel.

Jumlah partikel dalam 0,25 mol N2 sama dengan jumlah partikel dalam Mas Dayat
Mol - Rumus, Contoh Soal Dan Jawaban. Hubungan antara jumlah mol dan jumlah partikel adalah : Jumlah mol = jumlah partikel / L Jumlah Partikel (molekul) = jumlah mol x L Dengan L = bilangan avogadro = 6,02 x 10 pangkat 23 partikel/mol. Contoh soal: Berapa jumlah mol amonia (NH3) yang terdapat dalam 3,01 x 1026 molekul NH3 ? Jawaban:

Latihan Soal Kimia Hubungan Mol Dengan Jumlah Partikel Dan Menghitung Massa Molekul Relatif PDF
4. HUBUNGAN MOL DENGAN JUMLAH PARTIKEL. mol = jumlah partikel / 6,02 × 10 23 jumlah partikel = mol × 6,02 × 10 23 contoh soal ; 1). Diketahui HCL volumenya sebesar 48 L , tentuka berapa molekul senyawa HCL tersebut ! jawaban ; pertama - tama kita harus mencari nilai mol HCL RTP; mol = volume / 24 L = 48/24 = 2 mol

Contoh Soal Fraksi Mol Dan Pembahasannya
Contoh soal hubungan mol dengan jumlah partikel: 1). 1 mol besi (Fe) mengandung $ 6,02 \times 10^{23} \, $ atom. Berapakah jumlah atom besi yang terdapat dalam 2 mol besi? Penyelesaian : *). Diketahui :. Demikian pembahasan materi Hubungan Mol dengan Jumlah Partikel dan contoh-contohnya.
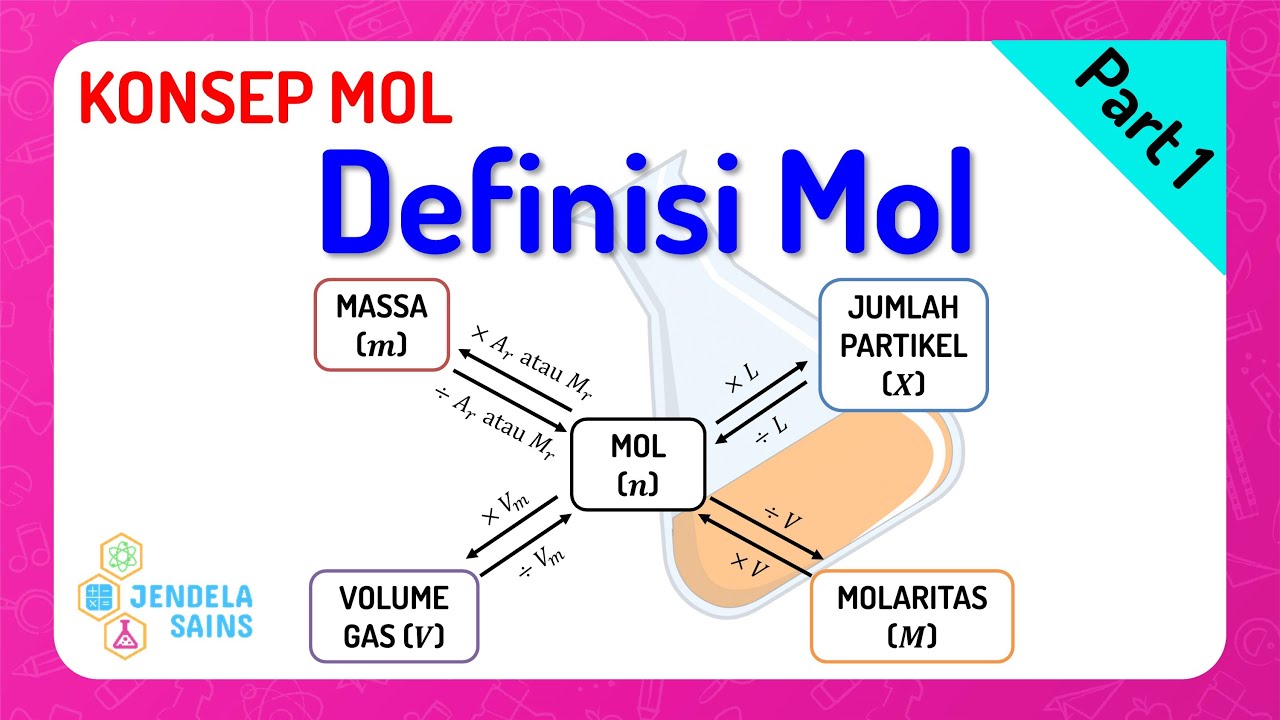
Konsep Mol Kimia Kelas 10 • Part 1 Hubungan Mol & Massa, Jumlah Partikel, Volume Gas, Molaritas
Berikut ini pembahasan soal tentang konsep mol yang menyatakan hubungan jumlah partikel dengan jumlah zat yang mempunyai satuan mol. Soal dalam tulisan ini bersumber dari Buku Sekolah Elektronik (BSE) Kimia 1 Untuk SMA/MA Kelas X oleh Budi Utami dkk, diterbitkan oleh Pusat Perbukuan Depdiknas 2009 pada halaman 99, Latihan 3.13.

Kumpulan Contoh Soal Konsep Mol dan Hubungannya dengan Jumlah Partikel, Massa Molar, dan Volume
Sedangkan nama Loschmdit dilambangkan sebagai simbol bilangan, yakni L. Lebih lanjut, berikut adalah contoh hubungan mol dengan jumlah partikel, yakni: Contoh, 1 mol unsur Fe = 6,02 x 10^23 atom Fe. ADVERTISEMENT. 1 mol NaBr = 6,02 x 10^23 molekul NaBr. 1 mol Cl2 = 6,02 x 10^23 molekul Cl2.

HUBUNGAN ANTARA MASSA, JUMLAH MOL, DAN JUMLAH PARTIKEL
Hubungan Mol dengan Jumlah Partikel, Massa Zat, Volume Zat, Rumus dan Contoh Penyelesaian Mol - Sahabat tentu pernah mendengar satuan dosin, gros, rim, atau kodi untuk menyatakan jumlah benda. Banyaknya partikel dinyatakan dalam satuan mol. Satuan mol sekarang dinyatakan sebagai jumlah partikel (atom, molekul, atau ion) dalam suatu zat. Para.

Kumpulan Contoh Soal Konsep Mol dan Hubungannya dengan Jumlah Partikel, Massa Molar, dan Volume
Mol merupakan jumlah partikel yang ada dalam sebuah zat, baik itu atom, molekul, atau ion. Ketika kita berbicara tentang hubungan antara mol dan jumlah partikel, kita perlu memahami konsep Avogadro. Konsep Avogadro mengatakan bahwa jumlah partikel dalam satu mol zat adalah konstan, dengan nilai sekitar 6,022 x 10^23.

Contoh Soal Konsep Mol Beserta Jawabannya Contoh Soal Terbaru
Rumusan Mol Hubungan mol (n) dengan Jumlah Parikel (JP) Dijelaskan bahwa 1 mol terdapat 6,02 x 10 23 atau jika dibuat rumusan: atau JP = n x L Keterangan: n = mol JP = Jumlah partikel L = bilangan avogadro (6,02 x 10 23) Contoh Soal: Tentukan jumlah mol Fe dari 3,01 x 10 22 atom Fe! Tentukan Jumlah molekul H 2 O dari 1,5 mol H 2 O!

Fraksi mol dan molalitas (m) Soal dan Pembahasan KIMIA KELAS 12 YouTube
Jadi, jumlah mol HCl yang dibutuhkan sama dengan jumlah mol NaOH, yaitu 3 mol. Dengan memperdalam pemahaman tentang konsep mol, kita dapat melakukan perhitungan kimia dengan lebih mudah dan akurat. Melalui penyelesaian dan pembahasan contoh soal, kita dapat meningkatkan kemampuan kita dalam menggunakan konsep mol dalam perhitungan kimia. Kesimpulan

Kumpulan Contoh Soal Konsep Mol dan Hubungannya dengan Jumlah Partikel, Massa Molar, dan Volume
Hubungan mol dengan jumlah partikel dapat dirumuskan: kuantitas (dalam mol) = jumlah partikel / NA atau jumlah partikel = mol x NA. Contoh soal: Suatu sampel mengandung 1,505 x 1023 molekul Cl2, berapa mol kandungan Cl2 tersebut? Jawab: Kuantitas (dalam mol) Cl2 = jumlah partikel Cl2 / NA = 1,505 x 1023 / 6,02 x 1023= 0,25 mol.

Soal Kimia Tentang Konsep Mol Satuan Jumlah Zat Read Master
Jawab: a) Gas O2 adalah unsur diatomik dengan partikel berupa molekul unsur. b) Banyaknya mol O2 yang mengandung 1,505 × 1023 partikel dapat kita hitung dengan menggunakan rumus berikut. Jumlah partikel = mol × N. mol = Jumlah partikel/N. mol = 1,505 × 1023/6,02 × 1023. mol =1,505/6,02. mol = 0,25 mol.

Soal Mol Penjelasan Lengkap dan Komprehensif tentang Mol dalam Kimia
Jadi, kamu bisa menyimpulkan bahwa 1 mol zat mengandung 6,02 x 10 23 partikel. Untuk itu, kamu bisa menyatakan hubungan antara jumlah mol dengan jumlah partikel yang ada di dalam senyawa menjadi: Jumlah mol X (n) = jumlah partikel X/L atau Jumlah partikel X = n x L. L merujuk pada bilangan Avogadro yang ditemukan oleh Johann Locshmidt pada 1856.