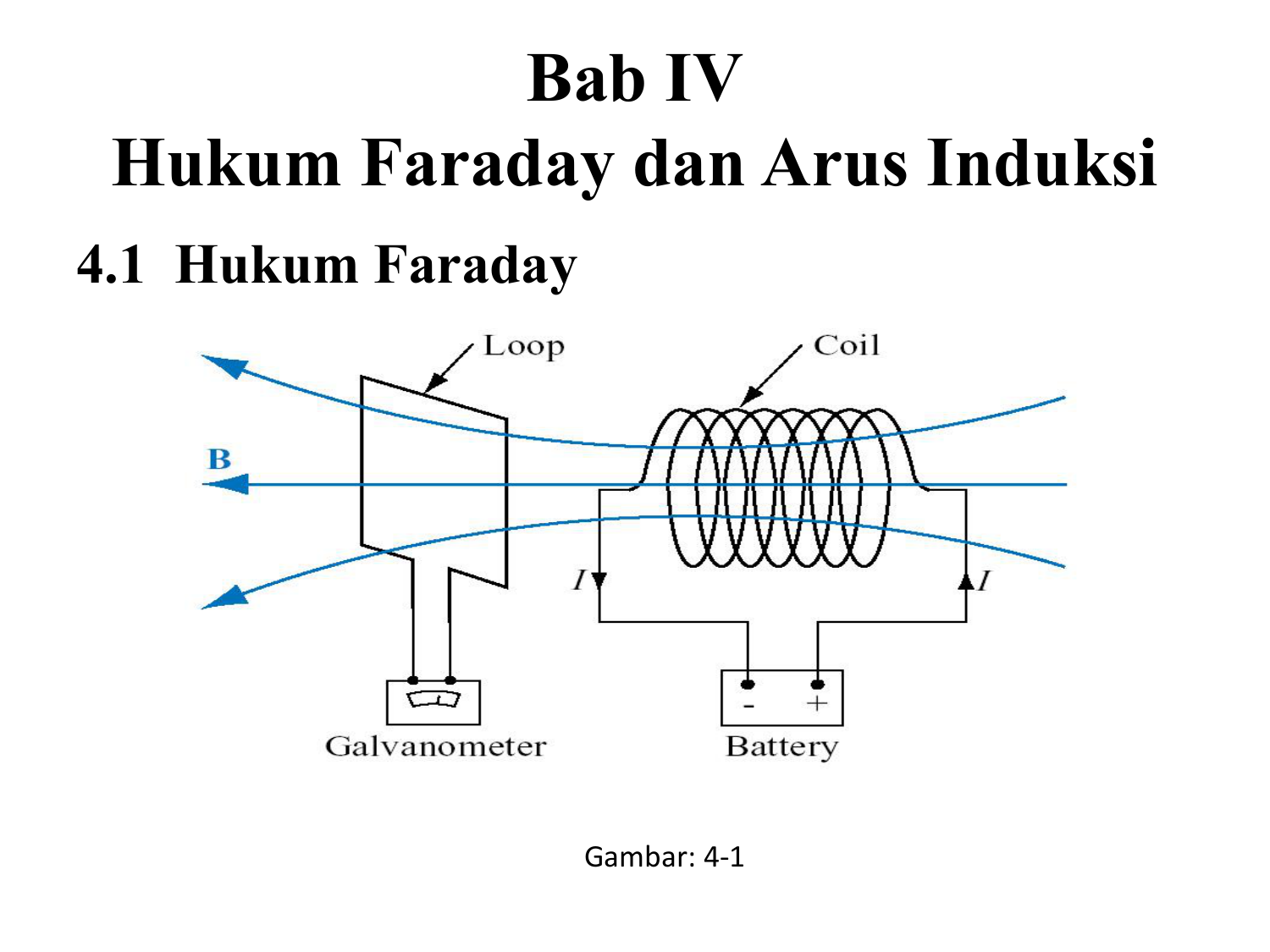
Hukum Faraday dan Arus Induksi
Rumus Hukum Faraday 1 Dan 2. Dalam sebuah Hukum Faraday, secara matematis perhitungan arus listrik dapat dirumuskan menjadi: Rumus Hukum Faraday untuk menghitung suatu gaya gerak listrik maka, rumus yang digunakan secara sistematis ialah sebagai berikut: ɛ = -N (ΔΦ / ∆t) Keterangan: ɛ ialah gaya gerak listrik (ggl) induksi (volt)

Hukum Faraday Kimia LEMBAR EDU
Mari kita lihat kembali Hukum Faraday 1 dan Hukum Faraday 2: Hukum Faraday 1 : w ≈ I x t. Hukum Faraday 2 : w ≈ ME. Jika digabungkan, kita peroleh w ≈ I x t x ME. Perbandingan ini menjadi persamaan dengan penambahan faktor 1/96.500, sehingga diperoleh rumus hukum faraday: w = 1/96.500 x I x t x ME. dengan, Contoh soal Hukum Faraday
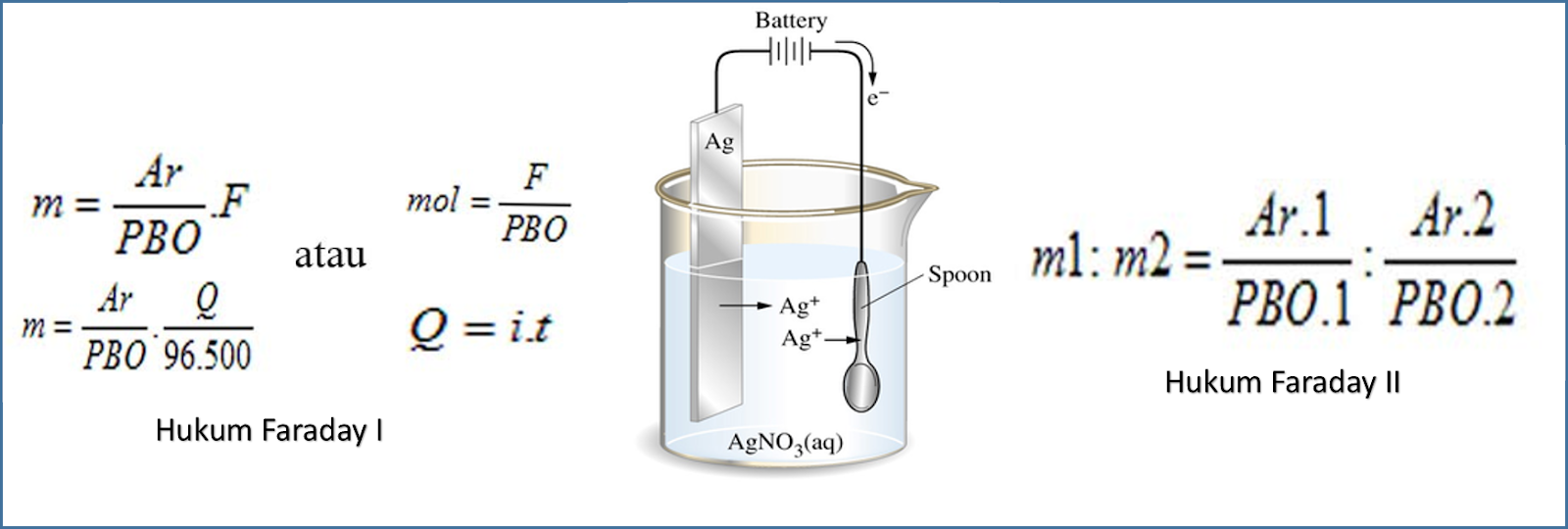
Hukum Faraday Pojok Kimia
Bunyi Hukum Induksi Faraday dan Pengaplikasiannya. by Mizzart Al Fatih. April 27, 2022. Kali ini, kita bakal mempelajari bunyi hukum Faraday yang terdapat di dalam hukum induksi Faraday. Selain itu, kita juga akan melihat pengaplikasiannya di dalam kehidupan sehari-hari. Sewaktu masih kecil dulu, gue tinggal di sebuah daerah yang sering banget.

Pembahasan Soal Elektrolisis Hukum Faraday 1 dan 2 YouTube
Bunyi Hukum Faraday 1 dan 2, Beserta Rumus Faraday. Bunyi Hukum Faraday - Pengertian Hukum Faraday adalah salah satu hukum yang menyatakan bahwa hubungan antara jumlah listrik yang dipakai dengan Massa Zat yang dihasilkan pada proses Elektrolisis baik di Katoda maupun Anoda, dan Teori Faraday ini sering disebut juga dengan Teori Kuantitatif.

Pengertian Hukum Faraday Dilengkapi Bunyi Rumus Dan Contoh Soal Riset
Rumus hukum faraday 2; Rumus hukum faraday 2 berbeda dengan rumus hukum faraday 1 sebab di sini ada massa ekuivalen dengan satuan ME dan juga massa zat dengan satuan w. Massa ekuivalen ini adalah hasil perhitungan massa atom relatif atau Ar yang dibagi dengan perubahan muatan ion atau bilangan oksidasinya. Jika ditulis dengan rumus maka akan.

Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Contoh Soal Hukum Faraday dan Pembahasan. 1. Berapa gram kalsium yang dapat dihasilkan dari elektrolisis lelehan CaCl 2 dengan elektroda grafit selama satu jam jika digunakan arus 10 A? (A r Ca = 40) Jawab: Massa Ca yang dihasilkan dapat dihitung dengan rumus: Diketahui i = 10 A; t = 1 jam = 3.600 s.
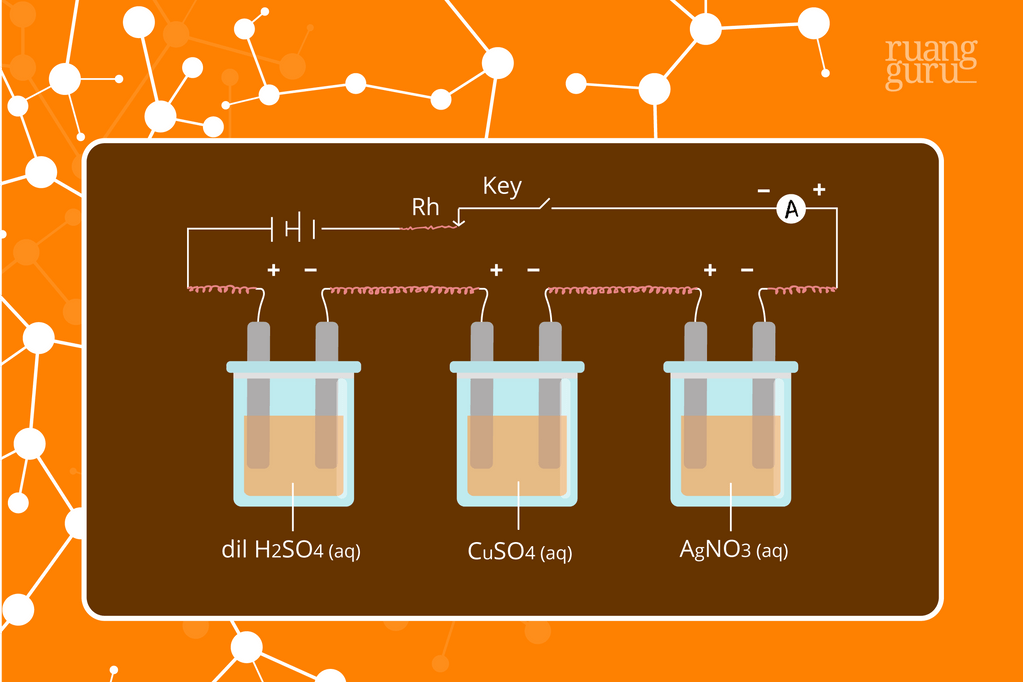
Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Bunyi Hukum Faraday 1 dan 2 Berikut Rumusnya. Hukum Faraday dirumuskan oleh ahli kimia dan fisika asal Inggris, Michael Faraday. Di tahun 1833, Faraday menjelaskan penemuan tentang aspek kuantitatif dari elektrolisis yang akhirnya menghasilkan dua hukum elektrolisis Faraday. Dikutip dari Modul Kimia XII yang disusun oleh Arni Wiyati (2020.

Hukum Faraday 1 dan Trik Mengerjakan Soalnya Kimia SMA Kelas 3 YouTube
Keterangan. W : Massa zat yang dihasilkan (gram) e : Massa ekuivalen. i : Kuat arus (ampere) t : Waktu (secon). F : Tetapan Faraday = 96.500 Coulomb/mol. 𝑄=𝑖×𝑡. Contoh soal penerapan Hukum Faraday 1 adalah sebagai berikut ini: 1.Tentukan Jumlah faraday untuk mereduksi ion Ca2+ dalam bentuk leburan (Ar Ca= 40) sebanyak 12 gram.
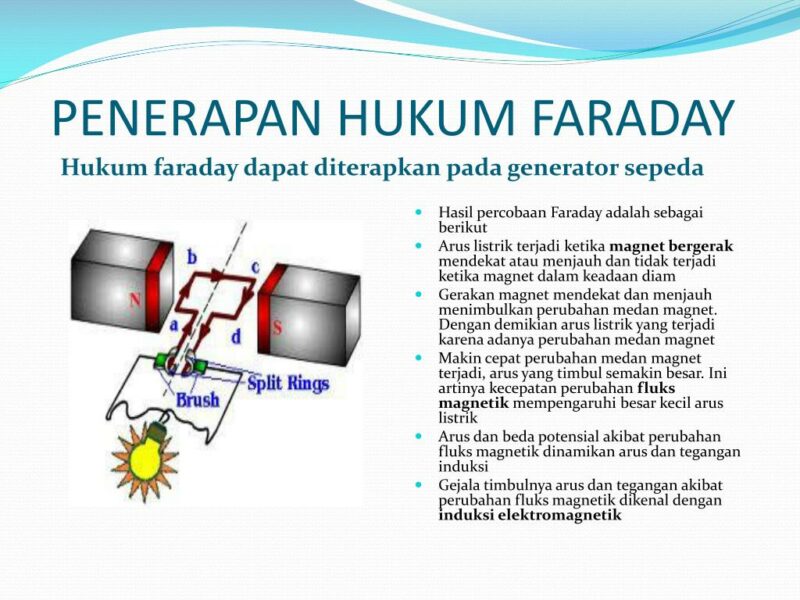
Hukum Faraday 1 Amp 2 Pengertian Rumus Dan Contoh Soal Riset
Hukum 1 Faraday. Hukum 1 Faraday berbunyi, "Massa zat yang dihasilkan oleh suatu elektrode selama elektrolisis(W) akan berbanding lurus dengan jumlah muatan listrik yang akan digunakan (Q)".Berikut ini merupakan persamaan untuk menyatakan Hukum 1 Faraday. W ~ Q. Jumlah muatan listrik yang digunakan (Q) sama dengan hasil kali antara kuat arus listrik (i) dan selang waktu (t).

Bunyi Dan Rumus Hukum Faraday 1 Dan 2 PDF
Pengertian dan Bunyi hukum Faraday 1 dan 2☑️ Rumus (persamaan), Contoh Soal dan pembahasan hukum Faraday 1 dan 2 lengkap☑️ Seorang ilmuwan yang berasal dari Inggris bernama Michael Faraday menemukan sebuah hukum yang digunakan dalam ilmu kimia dinamakan Hukum Faraday. Hubungan antara penggunaan muatan listrik dan hasil massa zat dalam electrode dijelaskan melalui hukum ini.

Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Berdasarkan percobaan yang dilakukannya tersebut, Michael Faraday menyimpulkannya dengan dua pernyataan seperti berikut ini yang juga sering disebut dengan Hukum Induksi Elektromagnetik Faraday 1 dan Hukum Induksi Elektromagnetik Faraday 2. Hukum Faraday 1. Setiap perubahan medan magnet pada kumparan akan menyebabkan gaya gerak listrik (GGL.

Hukum Faraday tentang GGL Induksi Induksi 1 YouTube
Materi ini bertujuan untuk memahami perhitungan sel elektrolisis dengan menggunakan hukum Faraday 1. Dengan adanya contoh dan latihan soal di harapkan faham.

Foto Hukum Faraday I dan II tentang Elektrolisis Halaman 1
Pada pertemuan ini kita bahas elektrolisis - hukum faraday 1 dan 2, Michael Faraday menemukan fakta bahwa banyaknya perubahan kimia yang dihasilkan oleh arus.

HUKUM FARADAY I DAN II KIMIA SMA YouTube
Hukum Faraday dibagi menjadi dua, yaitu Hukum Faraday 1 dan 2. 1. Hukum I Faraday. Hukum I Faraday berbunyi "Total zat yang dihasilkan pada elektroda, berbanding lurus dengan total muatan listrik yang mengalir melalui sel elektrolisis.". Arus listrik sebesar 0,2 ampere mengalir selama 2 jam melalui larutan Co (NO 3) 2.

Contoh Soal Hukum Faraday 1 LEMBAR EDU
Sebelum kita membahas contoh soal hukum faraday 2, mari kita ingat kembali bunyi Hukum Faraday II "massa zat yang dihasilkan berbanding lurus dengan massa ekuivalennya untuk jumlah listrik yang sama." Selanjutnya mari kita simak contoh soal hukum faraday 2 dan pembahasannya berikut ini. Soal No. 1 Pada elektrolisis larutan NiSO4 selama 45 menit menghasilkan endapan

Mengenal Bunyi Hukum Faraday Kimia Kelas 12
Adapun rumus hukum Faraday 1 dan 2 adalah sebagai berikut. Rumus Hukum Faraday 1. Ingat, bunyi hukum Faraday 1: "Massa zat yang dilepaskan selama elektrolisis berbanding lurus dengan jumlah listrik yang digunakan" Berdasarkan bunyinya, rumus hukum Faraday 1 dapat dituliskan sebagai berikut. G ≈ Q atau G ≈ it. Keterangan: