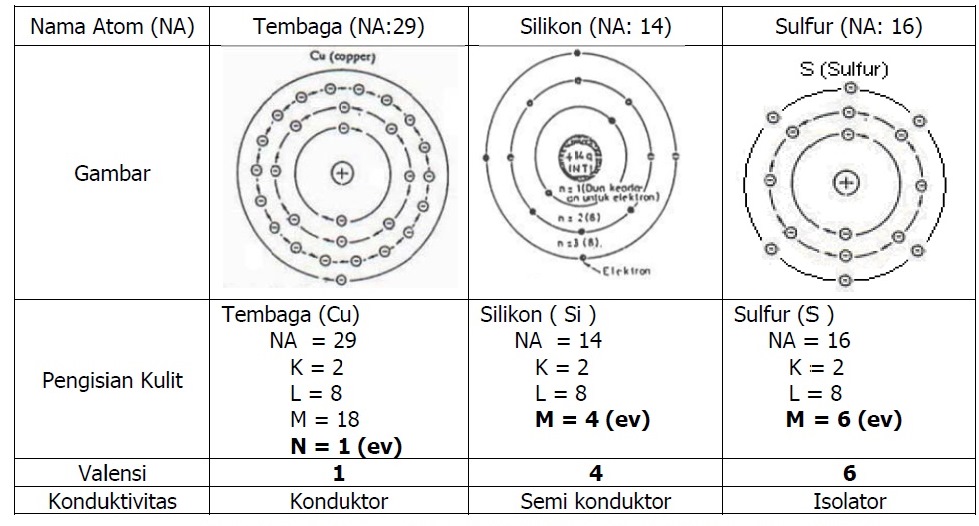
Teori Elektron Mekanik Alat Berat
Nah sekarang kita akan menggambarkan konfigurasi elektron memakai diagram orbital, teman. Sebenarnya gambarnya cukup mudah kok. Suatu subkulit punya sejumlah orbital. Orbital itu digambarkan sebagai persegi dan berisi garis setengah panah yang mewakili elektron. Subkulit s punya 1 orbital, p punya 3 orbital, d punya 5 orbital, dan f 14 orbital.

Jumlah Elektron Maksimum Pada Kulit P Adalah Cara Golden
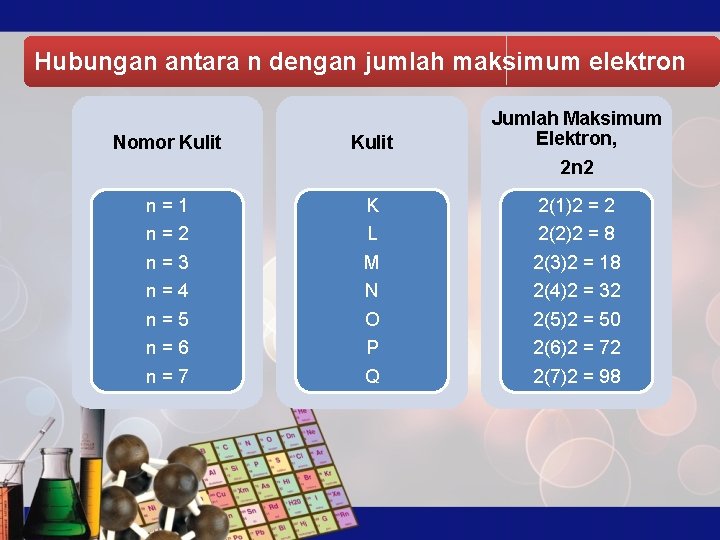
Konfigurasi elektron adalah penataan elektron ke dalam kulit dan subkulit atom. Sesuai pengertiannya, ada dua cara penulisan konfigurasi elektron,. Jumlah elektron maksimum yang bisa ditampung oleh kulit atom adalah 2n², dimana n adalah kulit ke-n.. yaitu aturan kedua. Jumlah elektron yang tersisa adalah 10, dimana 8 < 10 < 18, sehingga.

Jumlah maksimum elektron yang terdapat pada kulit M adala...
Diketahui unsur X dengan nomor atom 24, jumlah elektron maksimum pada orbital d adalah. A. 3 B. 4 C. 5 D. 6 E. 7 7. Jumlah elektron maksimum yang terdapat dalam kulit N adalah.. A. 8 B. 16 C. 32 D. 36 E. 42 8. Diketahui nomor atom Fe = 26, konfigurasi elektron ion Fe 3+ adalah.. A. 1s2 2s2 2p6 3s2 3p6 4s2 3d6 B. 1s2 2s2 2p6 3s2 3p6.
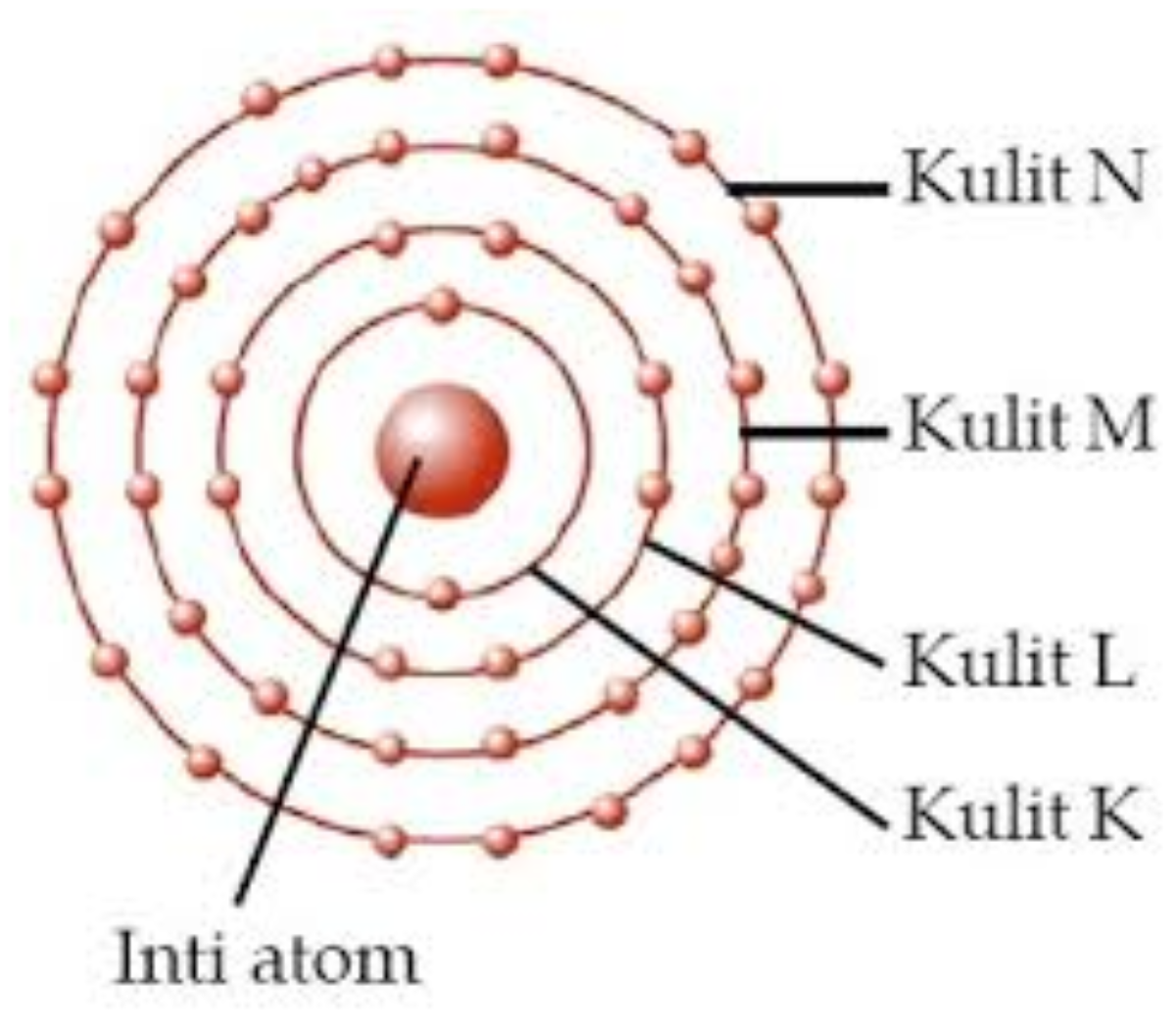
Memahami Kulit Elektron dan Aturan Dasar Penentuan Konfigurasinya Varia Katadata.co.id
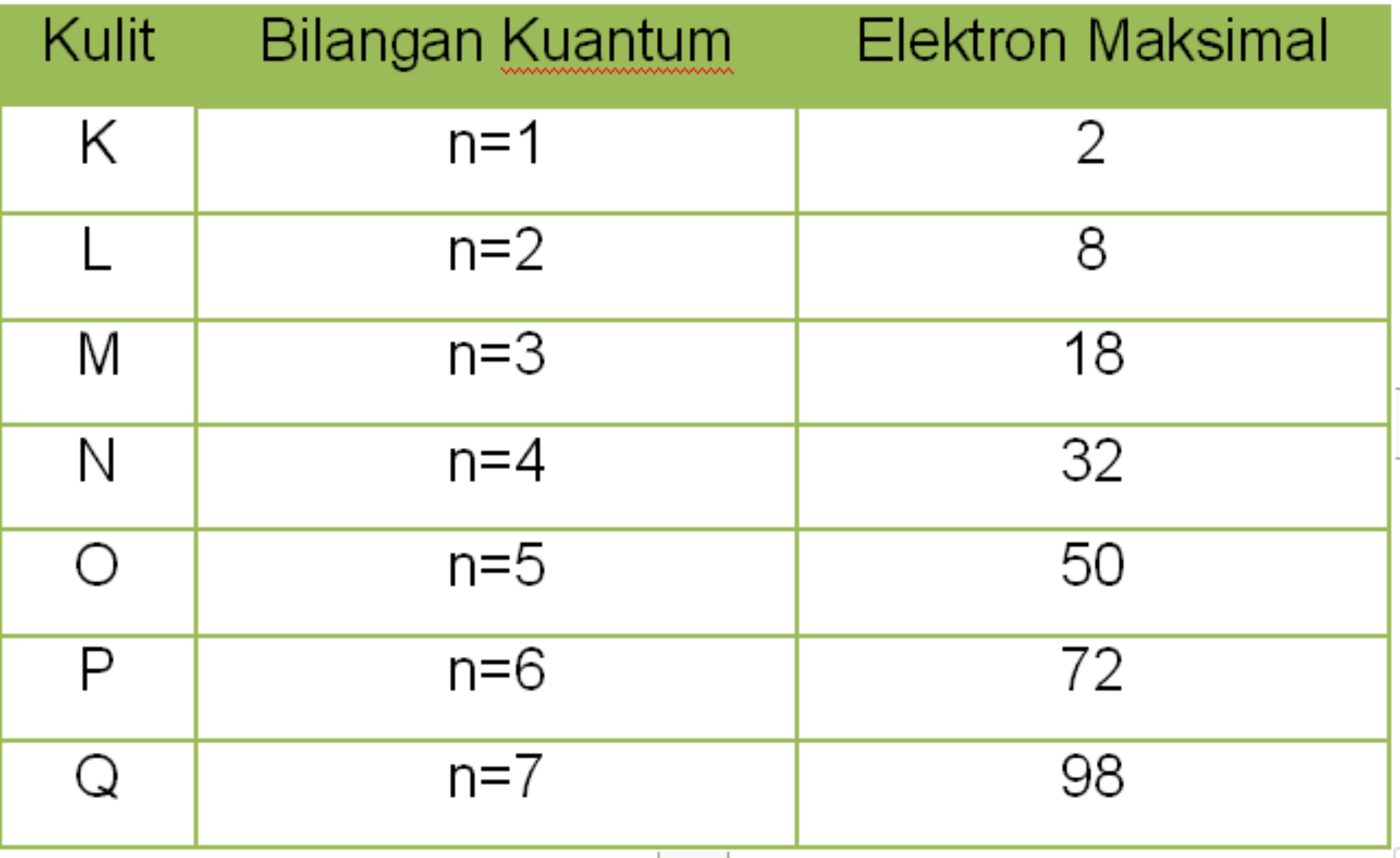
Jumlah maksimum elektron pada kulit N adalah 32. Untuk memahaminya, berikut adalah jumlah maksimum elektron pada setiap kulit atom!. Zat- zat yang Terkandung dalam Air Susu Ibu (ASI) Skola. 25/02/2024, 19:31 WIB. 3 Tugas MPR Sesuai UUD 1945. Skola. 25/02/2024, 19:00 WIB.
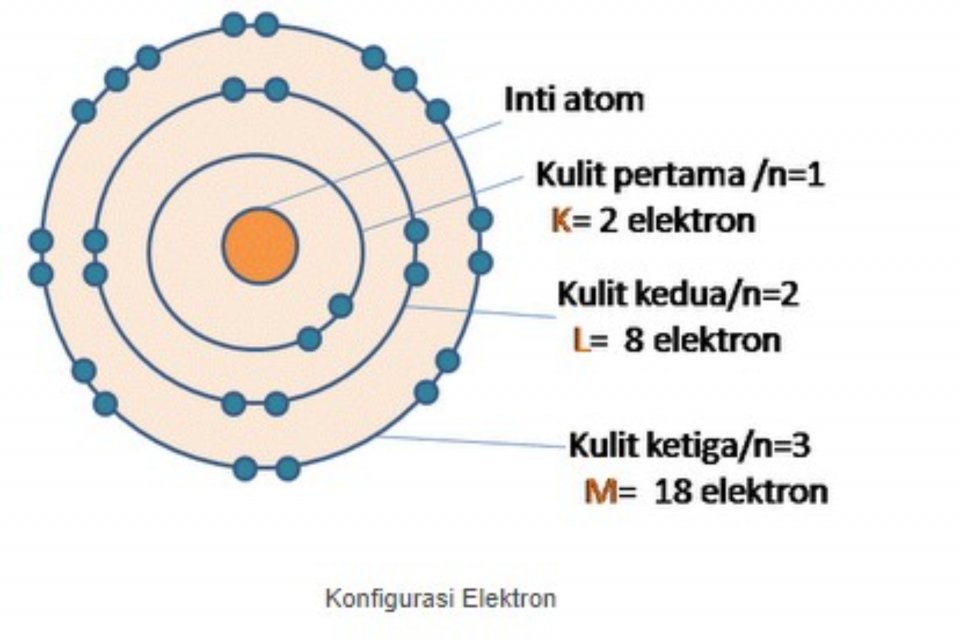
Memahami Kulit Elektron dan Aturan Dasar Penentuan Konfigurasinya Varia Katadata.co.id
Kulit ke-3 = 8 (bukan 10 meskipun jumlah maksimal pada kulit ke-3 = 18 karena kulit terluar tidak boleh melebihi 8 elektron) Kulit ke-4 = 2 (jumlah elektron tersisa, 20 - 18 = 2) Maka konfigurasi elektronnya adalah : 2 8 8 2. Timah (Sn) dengan nomor atom 50 berarti jumlah elektron = 50, maka jumlah elektron pada:

Jumlah Elektron Maksimum Dalam Kulit Atom Dengan N 3 Adalah JumlahID
Untuk menghitung jumlah elektron yang tersisa, Anda mengurangkan jumlah muatan dari nomor atomnya. Dalam kasus ion positif, jumlah proton lebih banyak daripada elektron. Misalnya, Ca 2+ memiliki muatan +2 sehingga ion kehilangan 2 elektron dari keadaan netralnya. Nomor atom kalsium adalah 20.
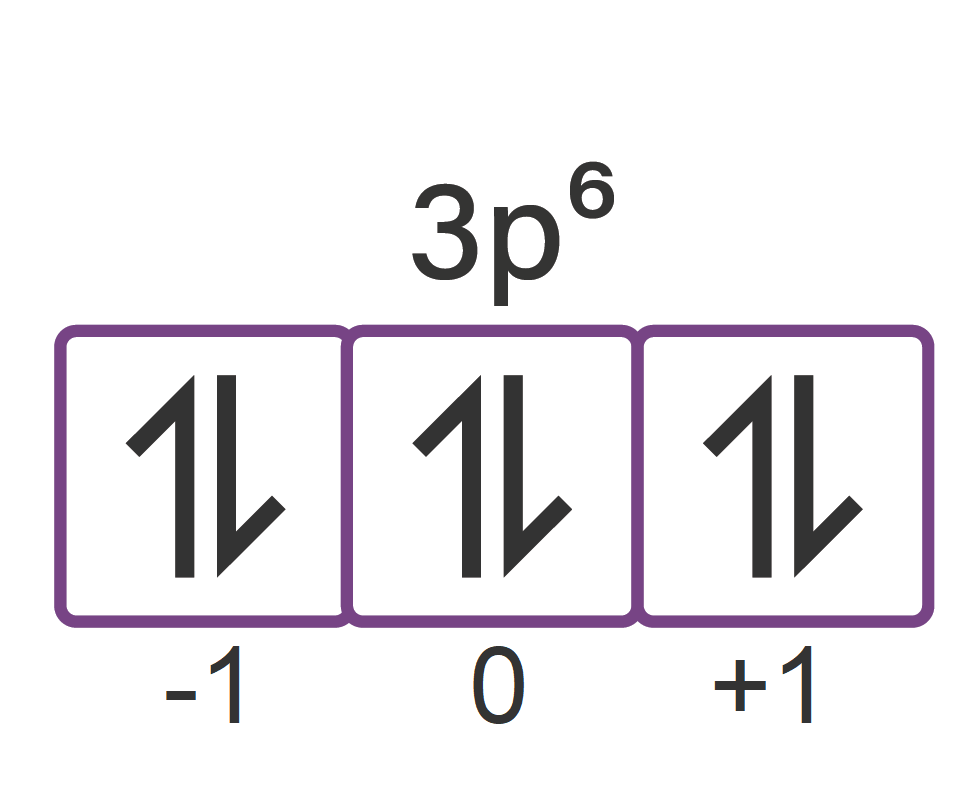
Dalam suatu atom, jumlah maksimum elektron yang me...
A. Istilah dalam Konfigurasi Elektron. 1. Kulit Elektron, Subkulit, dan Orbital. a. Kulit Elektron. Kulit elektron adalah lintasan tertentu yang memiliki tingkat energi tertentu yang ditempati oleh elektron-elektron suatu atom. Elektron pada atom menempati lintasan tertentu yang disebut dengan kulit elektron atau tingkat energi.

Jumlah maksimum elektron yang menempati kulit ketiga (n
Pembahasan. Jumlah elektron maksimum yang bisa ditampung oleh kulit atom adalah , dimana n adalah kulit ke-n. Kulit ke-1 dinamakan kulit K, kulit ke-2 dinamakan kulit L, dan seterusnya sesuai dengan urutan angka dan abjad. Kulit K maksimum berisi 2 elektron. Kulit L maksimum berisi 8 elektron. Kulit M maksimum berisi 18 elektron.

Jumlah Elektron Yang Menempati Kulit N Adalah pohon dadap daun dadap serep
Jumlah elektron maksimum yang terdapat pada kulit n adalah jumlah maksimal elektron yang dapat diakomodasi oleh sebuah kulit elektron pada orbital yang sama. Dalam notasi elektron, kulit n diwakili oleh huruf kecil "n" dan n merupakan bilangan bulat positif. Jumlah elektron maksimum dalam kulit n dapat dihitung menggunakan rumus 2n^2. Cara.
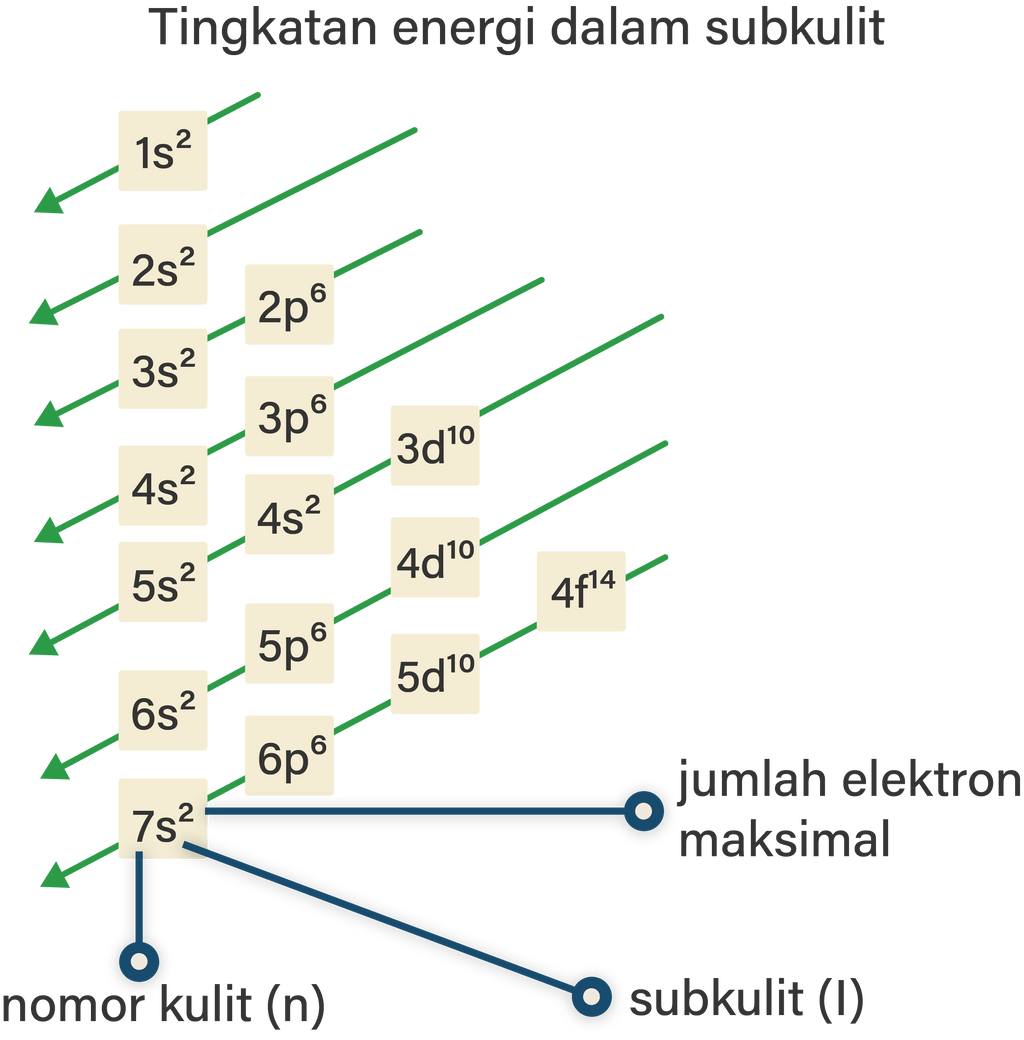
Jelaskan tentang konfigurasi elektron beserta cont...
Dalam kasus ini, jumlah maksimum elektron dalam kulit n = 3 adalah: 2 x (3^2) = 2 x 9 = 18 elektron. Jadi, dalam kulit n = 3, atom dapat menampung hingga 18 elektron. Dalam teori atom, pemahaman tentang jumlah elektron maksimum dalam kulit n memiliki peran penting dalam memprediksi sifat dan perilaku atom. Konsep ini juga mempengaruhi pemahaman.

Jumlah maksimum elektron yang terdapat pada kulit M adala...
Kulit yang paling dekat dengan inti atom adalah kulit K (n = 1) yang dapat ditempati paling banyak oleh 2 elektron. Semakin besar nomor kulit (n), jumlah elektron yang dapat menempati kulit tersebut akan semakin banyak.Urutan kulit dalam atom, yaitu: Kulit K = n = 1. Kulit L = n = 2. Kulit M = n = 3.

Menghitung Jumlah Proton, Elektron, dan Neutron dari Tabel Periodik KnK Land
Setiap kulit elektron hanya dapat terisi sejumlah tertentu elektron. Jumlah maksimum elektron yang dapat terisi pada kulit elektron ke-n adalah 2n 2, di mana n adalah nomor kulit atau bilangan kuantum utama.. Kulit K (n = 1) maksimum terisi 2 × 1 2 = 2 elektron.; Kulit L (n = 2) maksimum terisi 2 × 2 2 = 8 elektron.; Kulit M (n = 3) maksimum terisi 2 × 3 2 = 18 elektron.

Jumlah Elektron Yang Menempati Kulit N Adalah pohon dadap daun dadap serep
Pertanyaan. Jumlah maksimum elektron yang menempati kulit ketiga ( n = 3) dalam suatu atom adalah.. 10 elektron. 16 elektron. 18 elektron. 32 elektron. 40 elektron. Iklan. IS.

Konfigurasi elektron berdasarkan kulit Get Canva
Dengan demikian, agar jumlah elektron maksimum saat nilai m = +1, maka jumlah elektronnya adalah 9. Jumlah maksimum elektron pada saat n=3 dan m=+1, diagram orbital dengan l = 1 adalah 6, sedangkan l = 2 jumlah elektron maksimum nya adalah 9, namun pada opsi hanya tersedia pilihan 6, jadi jawabannya adalah 6 elektron. Jadi, jawaban yang benar.
Bab 1 Struktur Atom A Struktur Atom 1
Jumlah Elektron Maksimum pada Kulit n dalam Atom Besi. Pada atom besi, kulit n pada atomnya mampu menampung hingga 18 elektron berdasarkan aturan pengisian kulit elektron. Besi memiliki 26 proton dan 26 elektron dalam keadaan netralnya. Dalam hal ini, 18 elektron akan mengisi kulit n sehingga atom besi mencapai konfigurasi elektron yang stabil.
Memahami Kulit Elektron dan Aturan Dasar Penentuan Konfigurasinya Varia Katadata.co.id
Dalam kimia dan fisika atom, kelopak elektron atau kulit elektron dapat dianggap sebagai orbit yang dilalui elektron di sekitar nukleus atom. Kulit yang paling dekat dengan nukleus disebut "kulit 1 " (juga disebut "kulit K"), diikuti oleh "kulit 2 " (atau "kulit L"), kemudian "kulit 3 " (atau "kulit M"), dan seterusnya semakin jauh dari nukleus.