
senyawa polar keelektronegatifan, ikatan kimia, UN kimia 2016 pembahasan 03 YouTube
Pembahasan. Keelektronegatifan adalah kemampuan atau kecenderungan suatu atom untuk menangkap atau menarik elektron dari atom lain. Misalnya, fluorin memiliki kecenderungan menarik elektron lebih kuat daripada hidrogen. Jadi, dapat disimpulkan bahwa keelektronegatifan fluorin lebih besar daripada hidrogen. Konsep keelektronegatifan ini pertama.

Keelektronegatifan / Elektronegatifitas Suatu Unsur Adalah Sifat Yang Menyatakan tujuan dari
Keelektronegatifan adalah kemampuan suatu atom untuk menarik elektron ke dalam ikatannya ketika atomatom tersebut membentuk ikatan. Keelektronegatifan diukur dengan menggunakan skala Pauling yang besarnya antara 0,7 sampai 4. Yang mana, unsur yang mempunyai harga keelektronegatifan besar, cenderung menerima elektron dan akan membentuk ion.

Jelaskan Energi Ionisasi dan Keelektronegatifan? Fisika Kimia
Keelektronegatifan adalah konsep penting dalam kimia yang menggambarkan kemampuan suatu atom dalam menarik pasangan elektron dalam ikatan kimia. Konsep ini diperkenalkan oleh ilmuwan Linus Pauling pada tahun 1932 dan membantu kita memahami sifat ikatan kimia, kestabilan senyawa, dan polaritas molekul. Dalam artikel ini, kita akan menjelajahi.

Data keelektronegatifan beberapa unsur H=2,1;F=4,0;Cl=3...
Keelektronegatifan adalah sifat atom yang meningkat dengan kecenderungannya untuk menarik elektron ikatan. Jika dua atom terikat mempunyai nilai keelektronegatifan yang sama antara satu sama lain, mereka berkongsi elektron secara sama rata dalam ikatan kovalen. Biasanya, elektron dalam ikatan kimia lebih tertarik kepada satu atom (yang lebih.

PPT IKATAN KIMIA PowerPoint Presentation, free download ID6053258
Fluor adalah unsur yang paling elektronegatif dan sesium adalah unsur yang paling elektronegatif. Tabel Keelektronegatifan. Elektronegativitas adalah sifat kimia yang menggambarkan kekuatan atom dalam molekul untuk menarik elektron ke dirinya sendiri. Ada perbedaan besar dalam keelektronegatifan untuk atom dari sisi kiri dan kanan tabel periodik.

Diketahui data keelektronegatifan unsurunsur sebagai ber...
Keelektronegatifan (simbol χ) ialah satu sifat kimia yang menjelaskan kecenderungan suatu atom atau kumpulan berfungsi menarik elektron (atau kepadatan elektron) ke arahnya. [1] Keelektronegatifan suatu atom dipengaruhi oleh nombor atomnya dan jarak elektron valens daripada nukleus atom. Semakin tinggi nombor keelektronegatifan, semakin banyak.
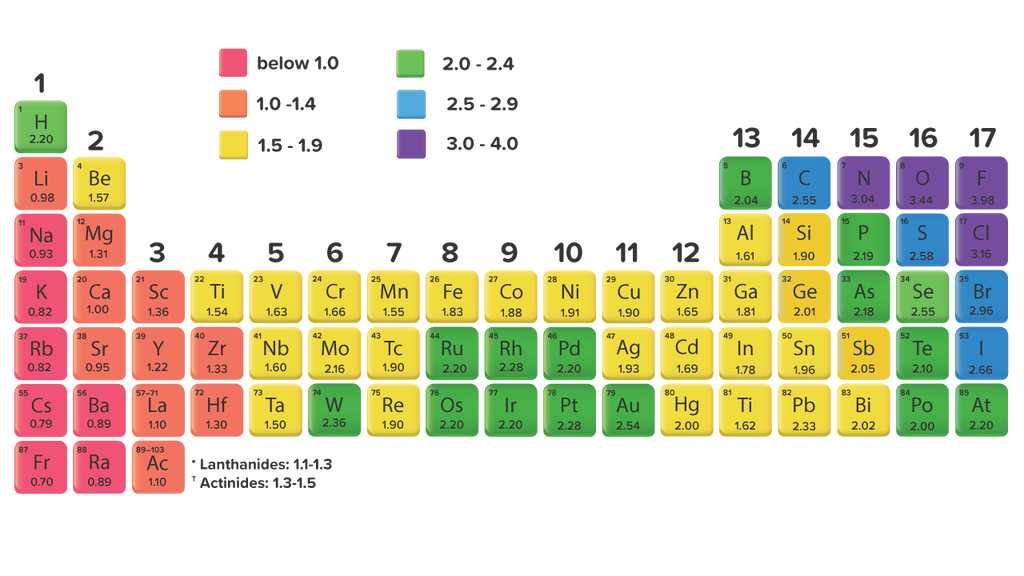
Unsur yang memiliki keeletronegatifan paling tingg...
Keelektronegatifan adalah ukuran kemampuan suatu atom untuk menarik elektron luarnya,atau elektron valensi. Karena elektron luar dari atom yang digunakan untuk ikatan, maka keeleketronegatifan berguna dalam meramalkan dan menerangkan kereaktifan kimia. Seperti jari-jari atom, keelektronegatifan dipengaruhi oleh jumlah proton dalam inti dan.

Diketahui keelektronegatifan unsur H, Cl, F dan Br secara berturutturut yaitu 2,1; 2,0; 4,0; 2
Elektronegativitas atau keelektronegatifan (Simbol: χ) adalah sebuah sifat kimia yang menjelaskan kemampuan sebuah atom (atau lebih jarangnya sebuah gugus fungsi) untuk menarik elektron (atau rapatan elektron) menuju dirinya sendiri pada ikatan kovalen. [1] Konsep elektronegativitas pertama kali oleh Linus Pauling pada tahun 1932 sebagai.

Keelektronegatifan / Elektronegatifitas Suatu Unsur Adalah Sifat Yang Menyatakan tujuan dari
Sedangkan, keelektronegatifan adalah kemampuan atom menarik elektron. Artinya, energi ionisasi dan keelektronegatifan adalah kebalikan. Dilansir dari Thought Co, atom dengan energi ionisasi yang rendah memiliki keelektronegatifan yang rendah juga karena inti atomnya tidak memberikan gaya tarik menarik yang kuat terhadap elektron.

Trik Super Kilat Memahami Keelektronegatifan
Keelektronegatifan Pauling, tanpa diragukan lagi, adalah skala yang paling luas dan digunakan, terutama dalam kursus kimia dasar atau kimia umum. Pada skala ini, nilai sewenang-wenang 4,0 ditetapkan untuk keelektronegatifan unsur paling elektronegatif dalam tabel periodik, fluor, dan nilai lainnya ditetapkan berdasarkan nilai referensi tersebut.

Apa itu Keelektronegatifan Kimia Atom YouTube
Kebalikan dari keelektronegatifan adalah elektropositif, jadi bisa dibilang cesium adalah elemen yang paling elektropositif. Perhatikan bahwa teks-teks yang lebih tua mencantumkan fransium dan cesium sebagai yang paling tidak elektronegatif pada 0,7, tetapi nilai untuk cesium secara eksperimental direvisi menjadi nilai 0,79..

Keelektronegatifan unsur dalam satu periodekimia sma YouTube
Keelektronegatifan adalah kemampuan suatu atom untuk menarik atom dari elektron lain mendekat ke arahnya. Nilai keelektronegatifan suatu atom dapat diketahui dengan melihat tabel periodik. Semakin ke kanan letak suatu atom pada tabel periodik, maka akan semakin besar pula nilai keelektronegatifan atom tersebut.

Cara Mudah Menjawab Soal Keelektronegatifan (Kimia SBMPTN, UN, SMA) YouTube
Keelektronegatifan adalah konsep dasar dalam kimia yang mengacu pada kemampuan atom untuk menarik elektron ke dirinya sendiri ketika membentuk ikatan kimia dengan atom lain.. Ini pertama kali diperkenalkan oleh Linus Pauling pada tahun 1930-an, dan telah terbukti menjadi alat yang berharga untuk memahami sifat dan perilaku unsur dan molekul..

Keelektronegatifan Adalah Suatu Bilangan Yang Menyatakan Kecenderungan Suatu Unsur Menarik
Keelektronegatifan adalah salah satu tren tabel periodik. Cara umum untuk mengukur keelektronegatifan adalah dengan menggunakan skala Pauling. Linus Pauling adalah seorang ilmuwan Amerika yang memenangkan Hadiah Nobel untukkimia dan perdamaian. Skala keelektronegatifan Pauling dapat dilihat pada Gambar 1 juga. Gambar 1.

Keelektronegatifan Terbesar YouTube
Pengertian Keelektronegatifan adalah sebuah konsep yang digunakan dalam kimia untuk menggambarkan kemampuan suatu atom dalam menarik elektron pada suatu ikatan kimia. Konsep ini pertama kali diperkenalkan oleh Linus Pauling pada tahun 1932 dan menjadi salah satu konsep penting dalam memahami sifat-sifat kimia suatu senyawa. Dalam.

Apa Itu Keelektronegatifan?
Definisi Keelektronegatifan yaitu kecenderungan suatu unsur untuk menarik eleektron sehingga bermuatan negatif. Nah dalam sebuah Sistem Periodik Unsur terdafat sifat keperiodikan atau ciri khas perubahan nilai keelektronegatifan unsur, berikut ini adalah Sifat-Sifat Keperiodikan Unsur terhadap Keelektronegatifan