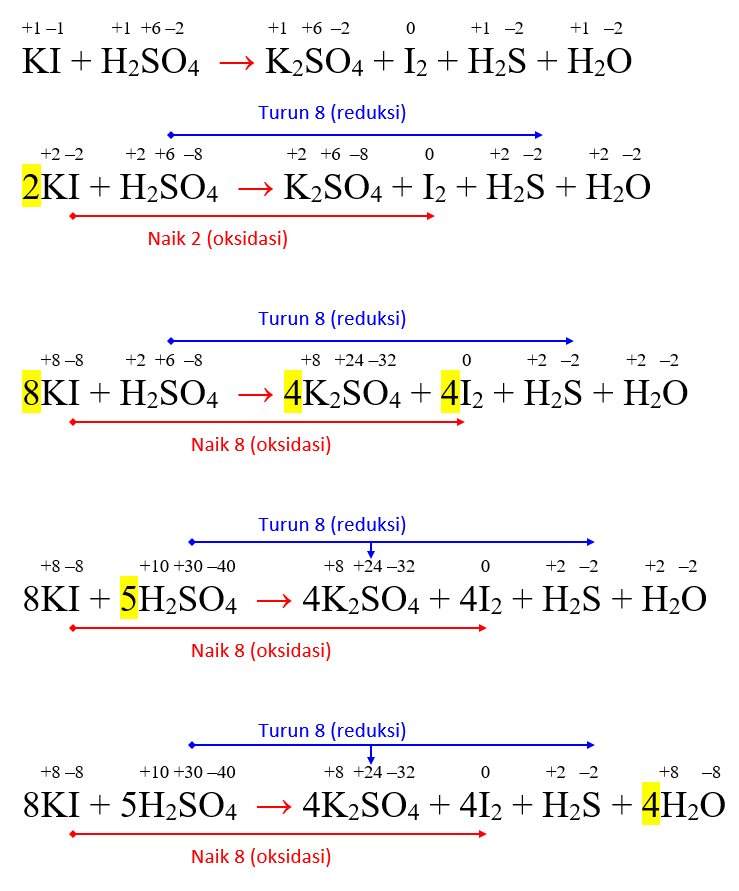
Penyetaraan Reaksi Redoks KI + H2SO4 → K2SO4 + I2 + H2S + H2O Markas Belajar
Pembahasan tergolong ke dalam senyawa kovalen polar, dimana akan mengalami ionisasi jika dilarutkan ke dalam air. Ionisasi asam sulfat akan menghasilkan 2 kation dan 1 anion . di dalam air akan terionisasi dengan reaksi: . Jadi, jawaban yang tepat yaitu A. Artikel Terkait: alat utama dalam pembuatan alat penjernih air sederhana terdiri atas
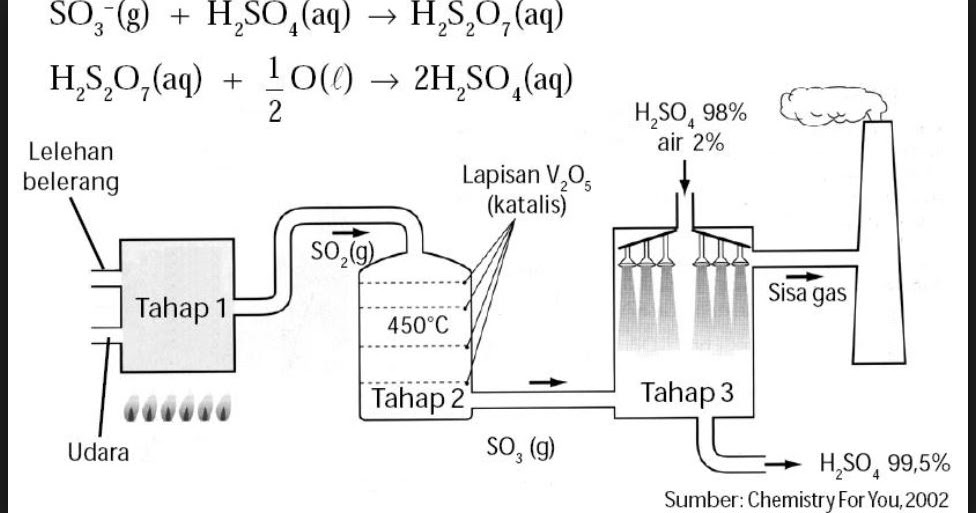
Sifat Reaksi Kegunaan Dan Pembuatan Asam Sulfat H2so4 Read Hstkb Riset
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Larutan H2SO4 di dalam a.

Berikut ini data hasil titrasi larutan H2 SO4 dengan laru...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Larutan H2SO4 di dalam a.
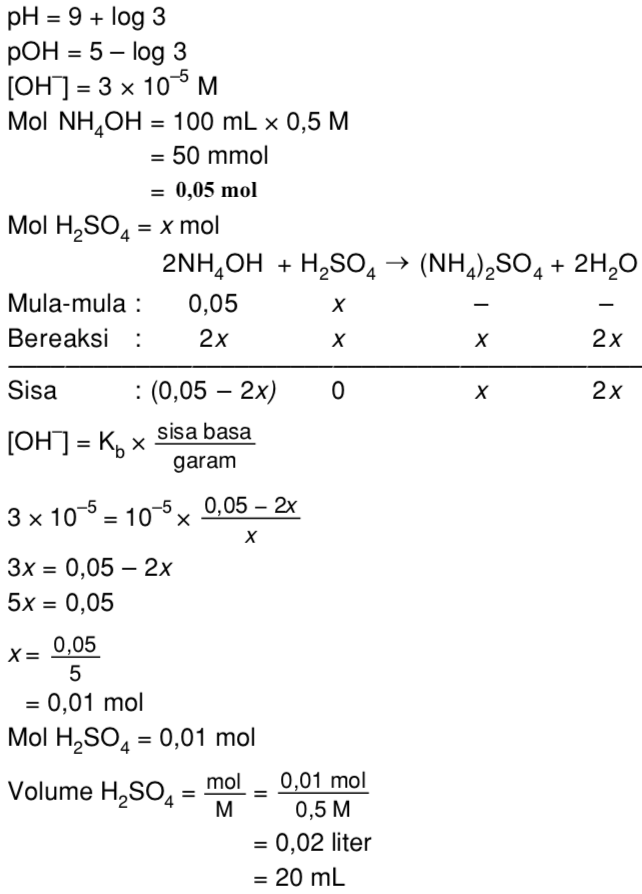
Berapa mL larutan H2SO4 0,5 M yang harus ditambahkan ke dalam 100 mL larutan NH4OH 0,5 M Mas Soal
Dijelaskan dalam Jurnal UNY, teori Arrhenius menyimpulkan: 1. Asam: zat/senyawa yang dapat menghasilkan H+ dalam air. HCl (aq) à H+ (aq) + Cl - (aq) 2. Basa: zat/senyawa yang dapat menghasilkan OH- dalam air. NaOH (aq) à Na+ (aq) + OH - (aq) • Reaksi netralisasi adalah reaksi antara asam dengan basa yang menghasilkan garam:

Larutan KCN dalam air akan bersifat basa, reaksi yang men...
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Larutan H2SO4 di dalam a.

Larutan H2so4 0 01 M Akan Memberikan Warna Yang Sama Ide Perpaduan Warna
Reaksi Asam Sulfat dan Air. Ketika Anda mencampur asam sulfat dan air, asam sulfat menyumbangkan ion hidrogen, menghasilkan ion hidronium. Asam sulfat menjadi basa konjugasinya, HSO 4 - . Persamaan reaksinya adalah: H 2 SO 4 + H 2 O → H 3 O + + HSO 4 -. Sangat penting untuk menambahkan asam sulfat ke air dan bukan air ke asam sulfat pekat.

50 mL larutan H2SO4 0,1 M direaksikan dengan 50 mL NH4OH
Reaksi hidrolisis adalah pencampuran larutan asam dengan larutan basa akan menghasilkan garam dan air. Reaksi Hidrolisis terjadi ketika suatu asam bertemu dengan basa yang akan menghasilkan garam dan air yang merubah pH dari campuran tersebut. Hidrolisis adalah reaksi kimia yang memecah molekul air (H2O) menjadi kation hidrogen (H+) dan anion hidroksida (OH−) melalui suatu proses kimia.

Larutan H2SO4 di dalam air akan terionisasi menjadi....
Pembahasan. H2SO4 tergolong ke dalam senyawa kovalen polar, dimana akan mengalami ionisasi jika dilarutkan ke dalam air. Ionisasi asam sulfat akan menghasilkan 2 kation H+ dan 1 anion SO42− . H2SO4 di dalam air akan terionisasi dengan reaksi: H2SO4(aq) 2H+(aq) + SO42−(aq).

Larutan NH4OH 0,1 M yang volumenya 400 mL ditambahkan ke dalam 200 mL larutan H2SO4, Mas Soal
Dengan begitu, kita bisa memperoleh rumus derajat ionisasi dari pengertian di atas sebagai berikut: Derajat ini digunakan untuk mewakili kekuatan suatu asam/basa. Elektrolit kuat akan memiliki derajat ionisasi sempurna, yaitu α=1. Kalau dalam persen berarti 100%. Elektrolit lemah akan memiliki derajat ionisasi 0<α<1, atau α=0,5.
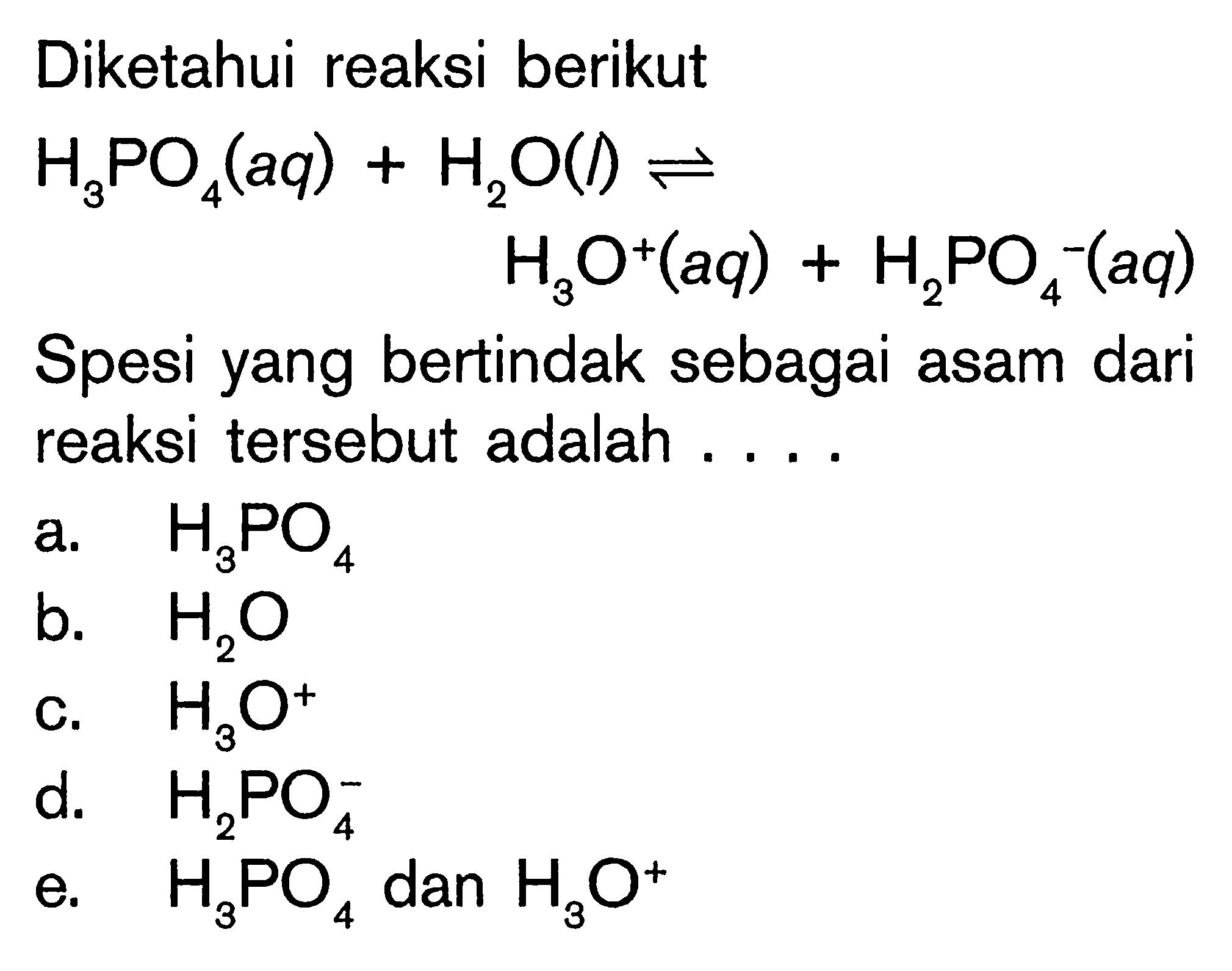
Sebutkan pasangan asambasa konjugasi dari reaksi berikut...
Dalam 1 mol H2SO4 terdapat 98 gram H2SO4. Jadi, jumlah mol H2SO4 dalam 500 gram larutan adalah: Jumlah mol = (500 g) / (98 g/mol) = 5.102 mol H2SO4. Menggunakan persamaan reaksi elektrolisis 2H2SO4 → 2H2 + O2, kita dapat mengetahui bahwa setiap 2 mol H2SO4 akan menghasilkan 2 mol H2 gas.

Untuk menentukan konsentrasi larutan H2SO4, larutan terse...
Menurut Arrhenius asam adalah senyawa yang meningkatkan konstentrasi H+ dalam larutan berair. Artinya, asam Arrhenius adalah senyawa yang menghasilkan ion hidrogen (H+). Ketika suatu zat dilarutkan dalam air. Jika zat tersebut menghasilkan ion H+, berarti zat tersebut adalah asam. Baca juga: Daftar Nama Asam-Basa Kuat dan Asam-Basa Lemah.

Hitunglah nilai pH dari larutan berikut! a. H2SO4 0,005 M b. 1mL H2SO4 0,1 M dalam 1 L air YouTube
Senyawa merupakan senyawa nentral sehingga ion-ion yang dihasilkan harus memiliki jumlah muatan netral atau nol (0). Senyawa akan terionisasi menjadi ion karena bilangan oksidasi maksimal dari hidrogen adalah +1 dan merupakan sisa asam oksi yang bermuatan -2, sehingga dapat jika dibuat menjadi persamaan reaksinya H 2 SO 4 → 2 H + + SO 4 2 − 0 = ( 2 × 1 ) + ( − 2 ) 0 = 0 Dari reaksi.

Larutan H2SO4 di dalam air akan terionisasi dengan reaksi...
H2SO4 adalah asam sulfat yang penting dan reaktif. Ketika dilarutkan dalam air, H2SO4 mengalami reaksi ionisasi membentuk ion hidrogen sulfat (HSO4-) dan ion sulfat (SO4²-). Reaksi ionisasi H2SO4 memiliki banyak aplikasi dalam industri dan laboratorium. Memahami reaksi ionisasi H2SO4 membantu kita dalam memahami sifat dan penggunaan asam.

Larutan H2SO4 0,05 M sebanyak 20 ml ditambah air sebanyak 180 ml. pH larutan tersebut akan YouTube
Iklan. Larutan H 2 SO 4 di dalam air akan terionisasi dengan reaksi.

Reaksi antara larutan kalium hidroksida dengan larutan as...
Pembahasan. Reaksi ionisisasi larutan di dalam air: Jadi, reaksi ionisasi larutan H2SO4 dalam air adalah H2SO4 → 2H+ + SO42−. Baca pembahasan lengkapnya dengan daftar atau masuk akun Ruangguru. GRATIS!

Percobaan titrasi antara 10 mL larutan H2SO4 dengan NaOH
Pada reaksi: 2Al(s) + 6HCl(aq) → 2AlCl₃(aq) + 3H₂(g) Berdasarkan reaksi di atas, pernyataan yang benar adalah.. A. 1 mol Al menghasilkan 67,2 liter gas H₂ pada keadaan standar B. 6 liter HCl menghasilkan 3 liter gas H₂ pada suhu dan tekanan yang sama C. 2 mol Al menghasilkan 67,2 liter gas H₂ pada keadaan standar D. 1 mol Al menghasilkan 33,6 liter gas H₂ pada keadaan standar.