
Rumus kimia garam yang benar berdasarkan tabel kation dan...
Garam yang bersifat asam akan bereaksi dengan ion hidrogen untuk membentuk asam dan basa. Reaksi ini umumnya dipresentasikan dalam persamaan reaksi. Persamaan reaksi hidrolisis untuk garam yang bersifat asam adalah sebagai berikut: R-X (s) + H2O (l) → R-H (aq) + X- (aq) Dimana R adalah sebuah gugus organik, X adalah garam asam.

Hubungan Yang Benar Antara Garam Dengan Perubahan Warna Pada Kertas Lakmus Adalah Sketsa
Larutan Asam. Sangat mudah menemukan senyawa asam dalam beragam barang sehari-hari, termasuk pada makanan, minuman, atau cairan pembersih rumah. Jeruk, lemon, dan tomat merupakan contoh buah dan sayur yang mengandung asam. Cuka dapur sebagai penambah rasa juga mengandung asam asetat. Aki pada kendaraan bermotor terdiri dari asam sulfat.

Pengertian asam basa dan garam berserta contohnya PR Sekolahku
Garam yang bersifat netral, memiliki pH = 7, berasal dari asam kuat dan basa kuat. Contoh: NaCl (natrium klorida), KI (kalium iodida), dan KNO 3 (kalium nitrat). Pengertian Larutan Garam, Sifat, Ciri, Jenis dan Contohnya : Adalah larutan yang didapat dari hasil reaksi asam dan basa. Garam merupakan suatu senyawa.

PH Hidrolisis ( Garam ) yang bersifat basa Kimia SMA YouTube
Oleh karena itu, larutan garam dari asam lemah dan basa kuat akan meningkatkan konsentrasi OH − dalam air sehingga larutannya bersifat basa (pH > 7).. Garam dari asam lemah dan basa lemah. Garam seperti CH 3 COONH 4 yang dapat terbentuk dari reaksi asam lemah (CH 3 COOH) dan basa lemah (NH 3) akan mengalami hidrolisis kation dan anionnya. pH larutan garam demikian bergantung pada kekuatan.

LENGKAP ‼️ Cara Mudah Menentukan Pasangan Asam Basa Konjugasi TeoriAsamBasa AsamBasaKonjugasi
Nilai Garam dari basa kuat dan asam lemah adalah pH > 7. Garam ini bersifat basa. Nilai Konsentrasi [OH -] adalah: Sedangkan garam yang terbentuk dari asam lemah dan basa lemah, sifat garamnya bergantung pada nilai ketetapannya masing-masing yaitu: Jika Ka = Kb. Maka garam tersebut bersifat netral atau pH = 7. Sedangkan Jika Ka > Kb

Contoh Garam Dari Asam Kuat Dan Basa Kuat Berbagai Contoh
1. Garam yang berasal dari asam kuat dan basa kuat. Garam seperti NaCl yang dapat terbentuk dari reaksi basa kuat (NaOH) dan asam kuat (HCl) tidak dapat terhidrolisis sehingga larutannya bersifat netral. Anion Cl − merupakan basa konjugasi yang sangat lemah karena berasal dari asam kuat sehingga cenderung tidak dapat menarik proton.

Pasangan spesi yang bersifat basa pada reaksi HCl + H2O ↔ H3O+ + Cl adalah YouTube
Pasangan garam yang bersifat basa ditunjukkan oleh nomor 1 dan 4. Jawaban (B). Dilansir dari buku Bahas Total Matematika, Fisika, Biologi, Kimia, Ekonomi, Geografi, Sosiologi SMA IPA Kelas XI (2011) oleh Budhi Setyono, garam K2CO3 atau kalium karbonat terbentuk dari asam lemah H2CO3 dan basa kuat KOH, sehingga memiliki pH > 7 atau bersifat basa.

Hidrolisis Garam Pengertian, Macam, Rumus, Dan Contoh Soal
Jika basa bereaksi dengan asam, maka dihasilkan senyawa 'garam'. Sifat yang umum pada senyawa basa dapat dilihat pada rasanya yaitu pahit serta jika diraba dengan jari akan terasa licin. Valensi basa adalah: jumlah ion OH- yang dilepaskan oleh 1 molekul basa. Contoh benda yang bersifat basa: - soda kue, - deterjen bubuk, - pasta gigi,
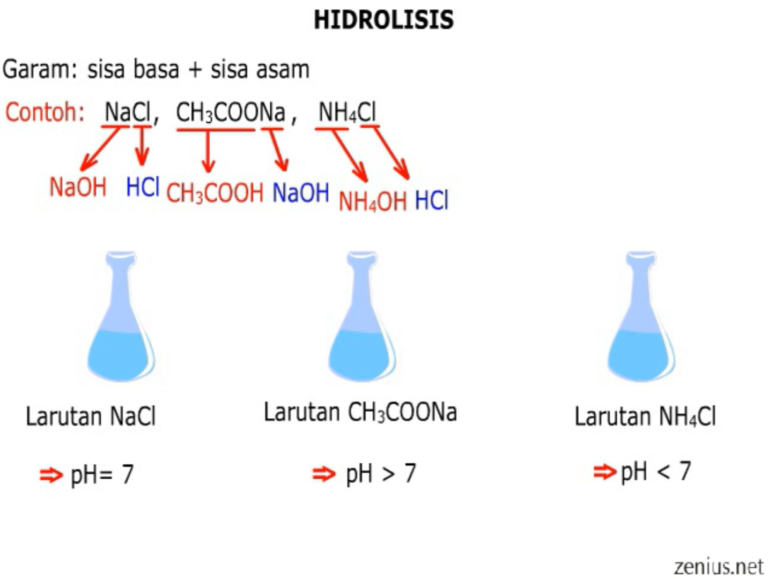
Pasangan Persamaan Reaksi Hidrolisis Untuk Garam Yang Bersifat Asam Adalah Homecare24
1. Multiple Choice. Pasangan garam yang bersifat basa ditunjukkan oleh nomor…. 2. Multiple Choice. 2.Berikut adalah hasilpengujian beberapa larutan garam dengan menggunakan lakmus. Percobaan Larutan Lakmus merah Lakmus biru. Garam yang mengalami hidrolisis dan sesuai dengan uji lakmusnya adalah . . . 3.

Pasangan garam berikut yang terhidrolisis sempurna dalam
CH 3 COONa adalah garam yang bersifat basa karena berasal dari CH 3 COOH ( asam lemah ) dan NaOH ( basa kuat ). Pasangan reaksi hidrolisis untuk garam yang bersifat asam adalah.. a. 1 dan 2. b. 1 dan 3. c. 2 dan 3. d. 3 dan 4. e. 4 dan 5 ( Kimia SMA XI, Unggul Sudarmo, Erlangga, 2013, h. 250 )

Pasangan persamaan reaksi hidrolisis yang bersifat basa adalah Universityku
Pasangan garam yang larutannya dalam air bersifat asam adalah…. A. (1) dan (2) B. (1) dan (3) C. (1) dan (4) D. (2) dan (3) E. (2) dan (4) Kunci Jawaban: E. Pembahasan: Na 2 CO 3 (garam ini berasal dari Asam Lemah dan Basa Kuat, sehingga sifat larutan adalah Basa) NH 4 NO 3 (garam ini berasal dari Asam Kuat dan Basa Lemah, sehingga sifat.

Perhatikan Tabel Berikut Pasangan Larutan Yang Bersifat Basa Adalah My XXX Hot Girl
Sehingga, hidrolisis garam adalah reaksi antara salah satu ion-ion garam (kation atau anion) dengan air dan membentuk larutan bersifat asam atau basa. Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut. Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya

Pasangan Garam Yang Bersifat Netral Ditunjukkan Oleh Nomor Homecare24
Berikut kami sajikan 10 soal hidrolisis garam dan mari kita bahas bersama-sama. Soal No 1. Terdapat larutan berikut: Na2CO3 NaCN NH4Cl CH3COONa KCl Pasangan garam yang bersifat basa ditunjukkan oleh nomor.. Pembahasan: Masih ingat kan, hidrolisis garam yang bersifat basa berasal dari asam lemah dengan basa kuat. Sekarang kita bahas satu-persata garam yang terbentuk.

Asam Basa Teori, Contoh, dan Sifat Asam Basa InformasainsEdu
Asam + basa → garam + air. HCl + KOH → KCl + H2O. Garam dapur (NaCl) diperoleh dari air laut yang mengalami penguapan dan kristalisasi. Untuk menjadikannya garam beryodium, harus diproses iodisasi (garam kalium/KI). Sifat-sifat atau ciri-ciri garam: Larut dalam air. Contohnya : KNO3, NH4Cl, Na2SO4. Sukar larut dalam air.

12 Contoh Asam Basa Dan Garam
Kesetimbangan Ion dan pH Larutan Garam; Garam yang Bersifat Basa; Terdapat larutan berikut: 1. Na2CO3 2. NaCN 3. NH4 Cl 4. CH3COONa 5. KCl Pasangan garam yang bersifat basa ditunjukkan oleh nomor.. Garam yang Bersifat Basa; Kesetimbangan Ion dan pH Larutan Garam; Kimia Fisik dan Analisis
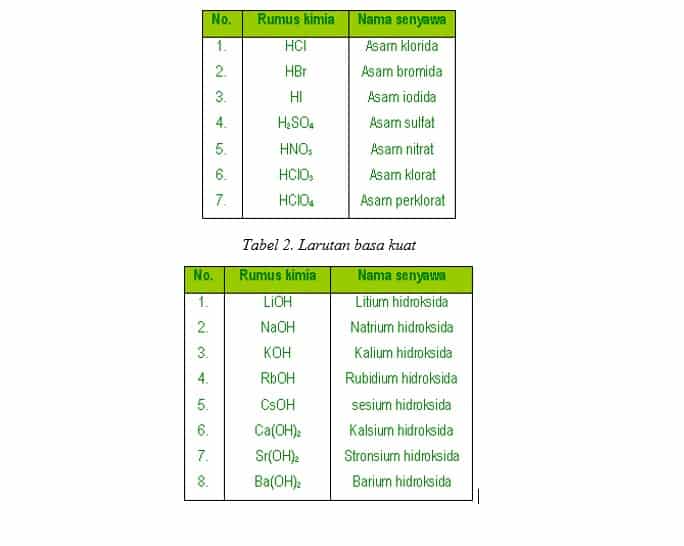
Contoh Garam Dari Asam Kuat Dan Basa Kuat Berbagai Contoh
Basa = penerima H+. Reaksi kimia yang bisa dijadikan contoh berdasarkan teori Bronsted-Lowry misalnya pada asam klorida (HCL) dan air (H2O) berikut ini: HCl + H2O ⇌ H3O+ + Cl-. Penjelasannya seperti mengutip pada emodul Kemdikbud: HCL bersifat asam karena itu ia mendonorkan ion H+ nya kepada H20. H20 bersifat basa karena ia menerima donor H+.