
pH campuran Asam Kuat dan Basa kuat Kimia SMA YouTube
pH campuran yang tidak akan berubah oleh pengaruh pengenceran adalah. a. CH3COOH (aq) + NH4Cl (aq) b.. Apakah semua campuran antara asam lemah basa konjugatnya. Tonton video. Tuliskan komposisi yang dapat membentuk: a. larutan penya. Tonton video. Jelaskan pengertian, sifat, dan fungsi larutan penyangga! Tonton video.

Kimia Kelas 11 Asam dan Basa (Menentukan pH campuran) YouTube
Berdasarkan konsentrasi ion H + di atas, diperoleh pH sebagai berikut. Jadi, pH yang terbentuk dari campuran kedua zat adalah 5 - log 4. Jawaban: 3. Contoh Soal 3. Pembahasan: Berdasarkan soal di atas, diketahui; b = Mol NH 3 = 50 mL x 0,2 M = 10 mmol g= Mol NH 4 Cl = 100 mL x 0,1 M = 10 mmol Valensi = 1 K b NH 3 = 1 x 10-5 Jawab:

Data trayek pH dan perubahan warna indikator ditunjukkan
Di dalam cairan lambung ini, yang bertindak sebagai larutan penyangga ternyata sangat kompleks, lho. Salah satu contohnya adalah campuran ion bikarbonat (HCO 3 -) dan ion karbonat (CO 3 2-). Campuran ini dapat mencegah perubahan pH yang drastis pada lambung, sehingga mencegah kerusakan lambung akibat pH makanan yang berubah-ubah. Misalkan.

pH larutan setelah penambahan H2SO4 dan pengenceran adalah Brainly.co.id
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!pH campuran yang tidak a.
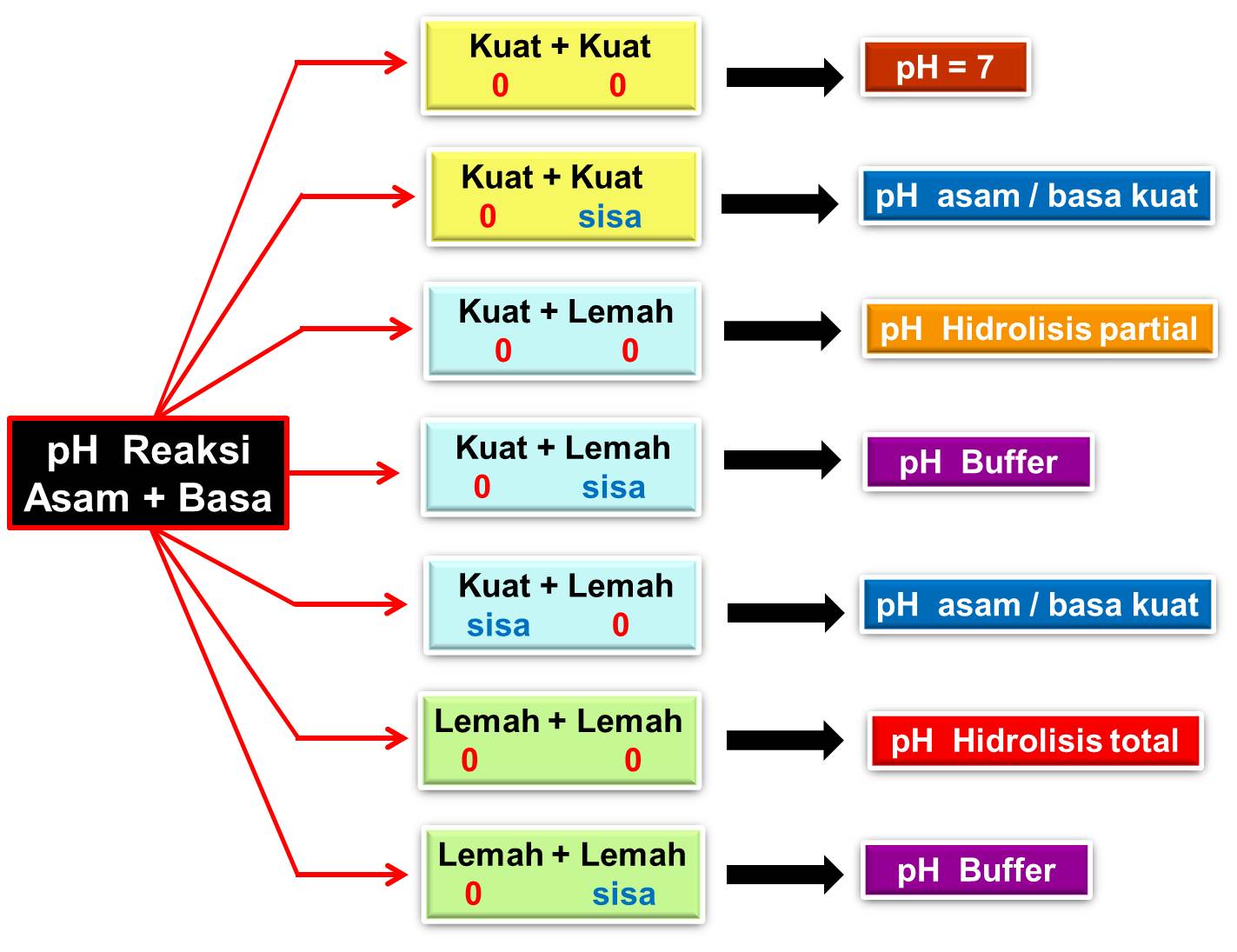
CINTA KIMIA PH REAKSI ASAM DAN BASA
Setiap pengenceran 100 kali dari volume semula maka pH berubah 2 satuan pH. Setiap pengenceran 1000 kali dari volume semula maka pH berubah 3 satuan pH. Setiap pengenceran 10.000 kali dari volume semula maka pH berubah 4 satuan pH. Demikian seterusnya tetapi tidak akan pernah melewati pH 7 dan hanya mendekati 7 atau hampir 7. Contoh Perhitungan.

Menghitung pH Campuran Asam Kuat dan Basa Kuat ( Asam Basa Kimia SMA Kelas 11 ) YouTube
Maka campuran yang tidak akan berubah oleh penambahan sedikit asam atau basa adalah (asam lemah) dengan (garam basa konjugasi). Jadi, jawaban yang benar adalah D. Larutan penyangga adalah suatu sistem larutan yang dapat mempertahankan nilai p H agar tidak terjadi perubahan yang berarti oleh penambahan sedikit asam atau basa.

Hitunglah pH campuran antara 200 mL larutan HNO2 0,15 M dengan 150 mL larutan KOH 0,10 M (Ka
Penambahan basa (OH −): ion OH − dari asam yang ditambahkan akan bereaksi dengan komponen asam konjugasinya. Misal larutan buffer basa NH3 / NH + 4: NH3 + H + ⇄ NH + 4 NH + 4 + OH − → NH3 + H2O. -. pengenceran: pada pengenceran hanya memperbesar volume komponen-komponen larutan penyangga.
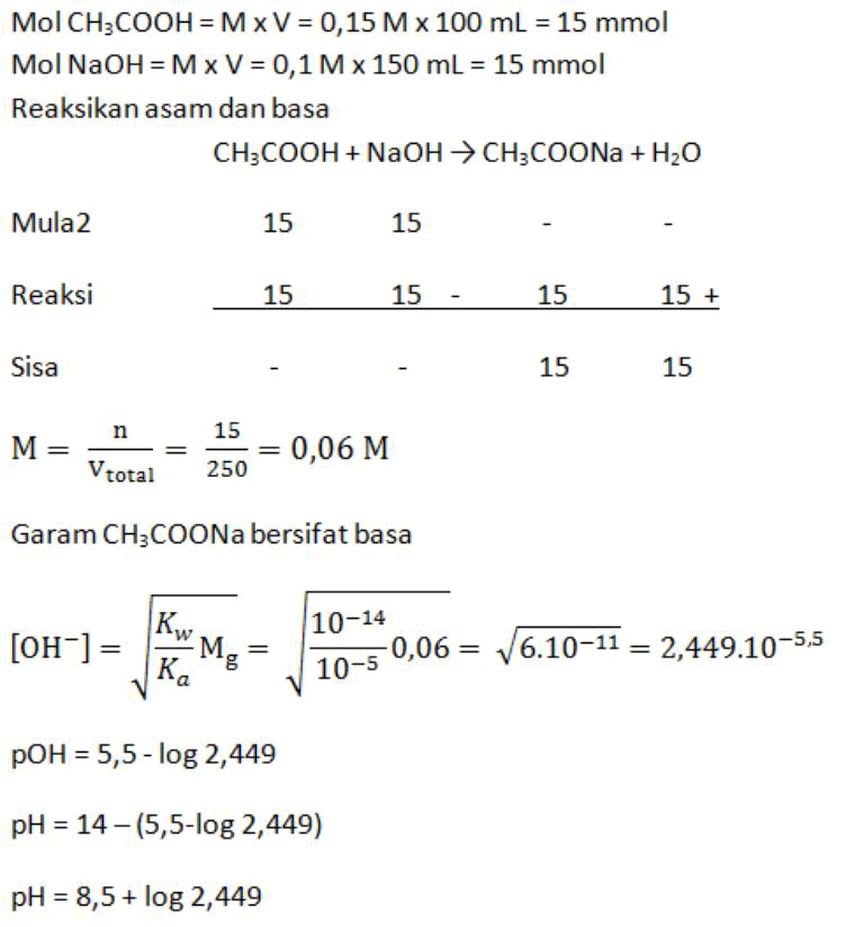
Larutan CH3COOH 0,15 M yang volumenya 100 mL dicampur dengan 150 mL larutan NaOH 0,1 M (Ka
Iklan. Pertanyaan. pH campuran berikut yang tidak akan berubah oleh penambahan sedikit asam atau basa adalah. asam asetat dengan amonium klorida. asam asetat dengan natrium klorida. asam sulfat dengan natrium sulfat. asam asetat dengan amonium sulfat. asam asetat dengan natrium asetat. Iklan.

Identifikasi Asam Basa
P asangan larutan yang pH-nya tidak akan berubah apabila ditam bah sedikit. sehingga pH campuran = 8 adalah. a. 66 gr. b. 33 gr. c. 13,2 gr. a. pH larutan penyangga berubah oleh.

pH Campuran asam Lemah dan Asam KuatKimia SMA YouTube
Istilah "pH" berasal dari kata Jerman "potenz," yang berarti "pangkat" , dikombinasikan dengan H, simbol unsur untuk hidrogen, jadi pH adalah singkatan dari "pangkat hidrogen.". Pengertian pada umumnya, pH (Power of Hydrogen) adalah skala yang digunakan untuk menyatakan tingkat keasaman atau kebasaan yang dimiliki oleh suatu larutan.. Skala dari pH terdiri dari angka 1 hingga
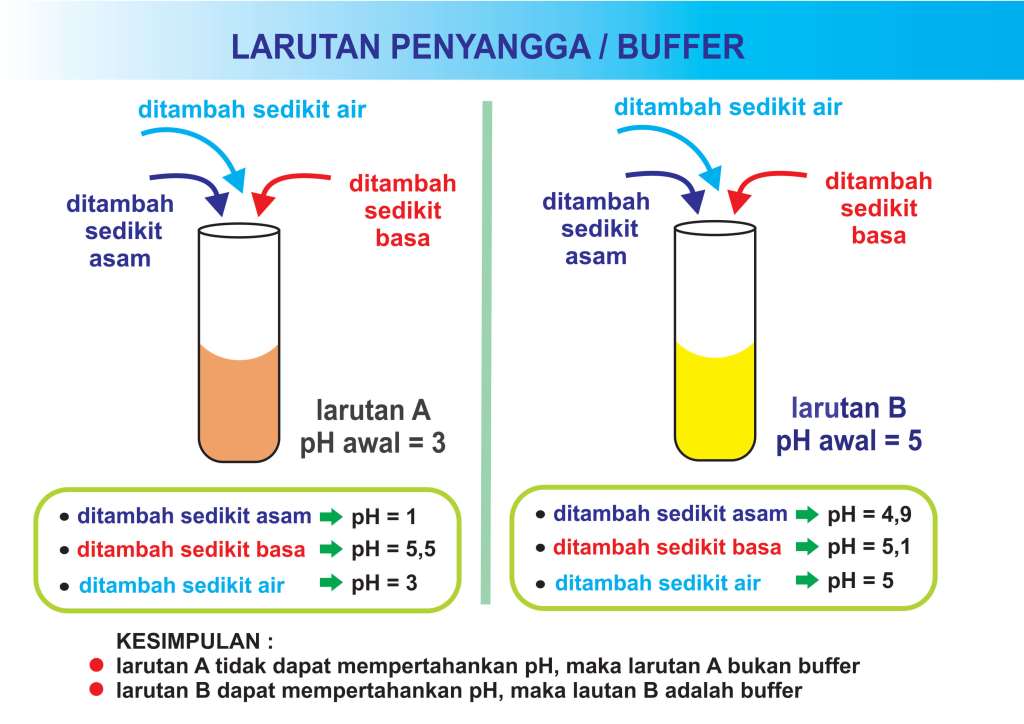
Contoh Soal Ph Larutan Penyangga
Pembahasan. Suatu larutan yang tidak akan berubah pHnya meskipun diencerkan adalah larutan penyangga. Larutan penyangga terdiri dari asam/basa lemah dan garam atau konjugatnya. Makan pasangan yang sesuai adalah . Campuran kedua senyawa tersebut dapat membuat larutan penyangga.

PH PENGENCERAN DAN CAMPURAN YouTube
tidak melakukan eliminasi. Fungsi utama sistem buffer adalah mencegah perubahan pH yang disebabkan oleh pengaruh asam fixed dan asam organic pada cairan ekstraseluler. Sebagai buffer, sistem ini memiliki keterbatasan yaitu4: a. Tidak dapat mencegah perubahan pH di cairan ekstraseluler yang disebabkan karena peningkatan CO 2. b.

Cara Menghitung Ph Larutan Asam Kuat Dan Asam Lemah Panduan Kimia Riset Sexiz Pix
Halo Shalma, Kakak bantu jawab ya. Jawaban yang benar adalah D. Larutan penyangga adalah suatu sistem larutan yang dapat mempertahankan nilai pH larutan agar tidak terjadi perubahan pH yang berarti oleh karena penambahan asam atau basa maupun pengenceran. Larutan ini disebut juga dengan larutan buffer atau dapar. Komponen Larutan Penyangga: 1.

Hitunglah pH campuran antara 200 mL larutan HNO2 0,15 M dengan 150 mL larutan KOH 0,10 M (Ka
Nilai pH air dari yang tadinya sesuai bagi makhluk hidup di dalamnya akan berubah akibat zat pencemar tersebut. Oleh karena itu, penting untuk mencegah dan mengendalikan faktor yang mempengaruhi pH air agar tetap terjaga kualitasnya. Berikut ini adalah faktor-faktor yang mempengaruhi pH air: Konsentrasi CO 2 dalam air

Soal Pembahasan Larutan Penyangga Buffer Reaksi Asam Basa Lemah Dan Hot Sex Picture
Larutan penyangga memiliki pH yang konstan, terhadap pengaruh pengenceran atau ditambah sedikit asam atau basa. Secara teoritis berapa pun diencerkannya pH tidak akan berubah, tetapi dalam praktiknya jika pengenceran besar sekali, jelas pH-nya akan berubah.. Bila 50 mL larutan NH4OH 0,2 M dicampurkan ke dalam 50 mL larutan HCl 0,1 M. Hitung.

Pasangan campuran larutan yang dapat membentuk larutan pe...
Larutan penyangga atau larutan buffer adalah larutan yang mampu mempertahankan pH tertentu terhadap usaha mengubah pH, seperti penambahan asam, basa, ataupun pengenceran. Dengan kata lain, pH larutan penyangga tidak akan berubah walaupun pada larutan tersebut ditambahkan sedikit asam kuat, basa kuat atau larutan tersebut diencerkan. Misalnya.