
Molaritas Pengertian, Rumus, Pembuatan, Pengenceran Larutan Dan Contohnya Lengkap BprsKu.Co.Id
Contoh perhitungan molaritas larutan. Misalnya 0,25 liter larutan urea (CO(NH2)2) dibuat dengan cara melarutkan 3 gram urea dalam air. Massa molekul relatif urea adalah 60. Molaritas larutan urea bisa dihitung dengan cara : Jumlah mol urea, n = gram/Mr = 3/60 = 0,05 mol Molaritas larutan, M = n/V = 0,05/0,25 = 0,2 molar

Massa Jenis dan Cara Mengukurnya Fisika SMP
Ingat, rumus molaritas pencampuran adalah: Maka, konsentrasi larutan setelah dicampurkan adalah: M campuran = (100 x 0,1) + (150 x 0,2) / (100 + 150) = 40 / 250. = 0,16 M. Quipperian, itu dia pembahasan mengenai rumus molaritas beserta contoh soal dan pembahasannya. Agar semakin paham dan mahir dalam menggunakan rumus molaritas, cobalah untuk.

Pengertian Dan Rumus Molaritas Dan Contoh Soal Molaritas Lengkap Riset Riset
Rumus Molaritas. Molaritas termasuk konsentrasi larutan. Dari berbagai bentuk konsentrasi yang dipengaruhi sifat koligatif larutan yaitu molaritas, molalitas, dan fraksi mol. Satuan molaritas adalah mol/liter atau M. Rumus molaritas yaitu mol zat terlarut dibagi volume larutan. Tetapi, molaritas dapat dicari melalui massa jenis zat terlarut dan volume larutan.
Pahami Rumus Molaritas, Contoh Soal, dan Pembahasannya Berikut Ini
Molaritas gula (C12H22O11) = 0,015 mol / 0,1 L = 0,15 M. Itulah cara menghitung molaritas dengan massa jenis. Dengan menggunakan rumus ini, kita bisa menghitung konsentrasi larutan dengan mudah. Namun, perlu diingat bahwa rumus ini hanya berlaku untuk larutan yang bersifat homogen dan zat terlarutnya tidak bereaksi dengan pelarut.
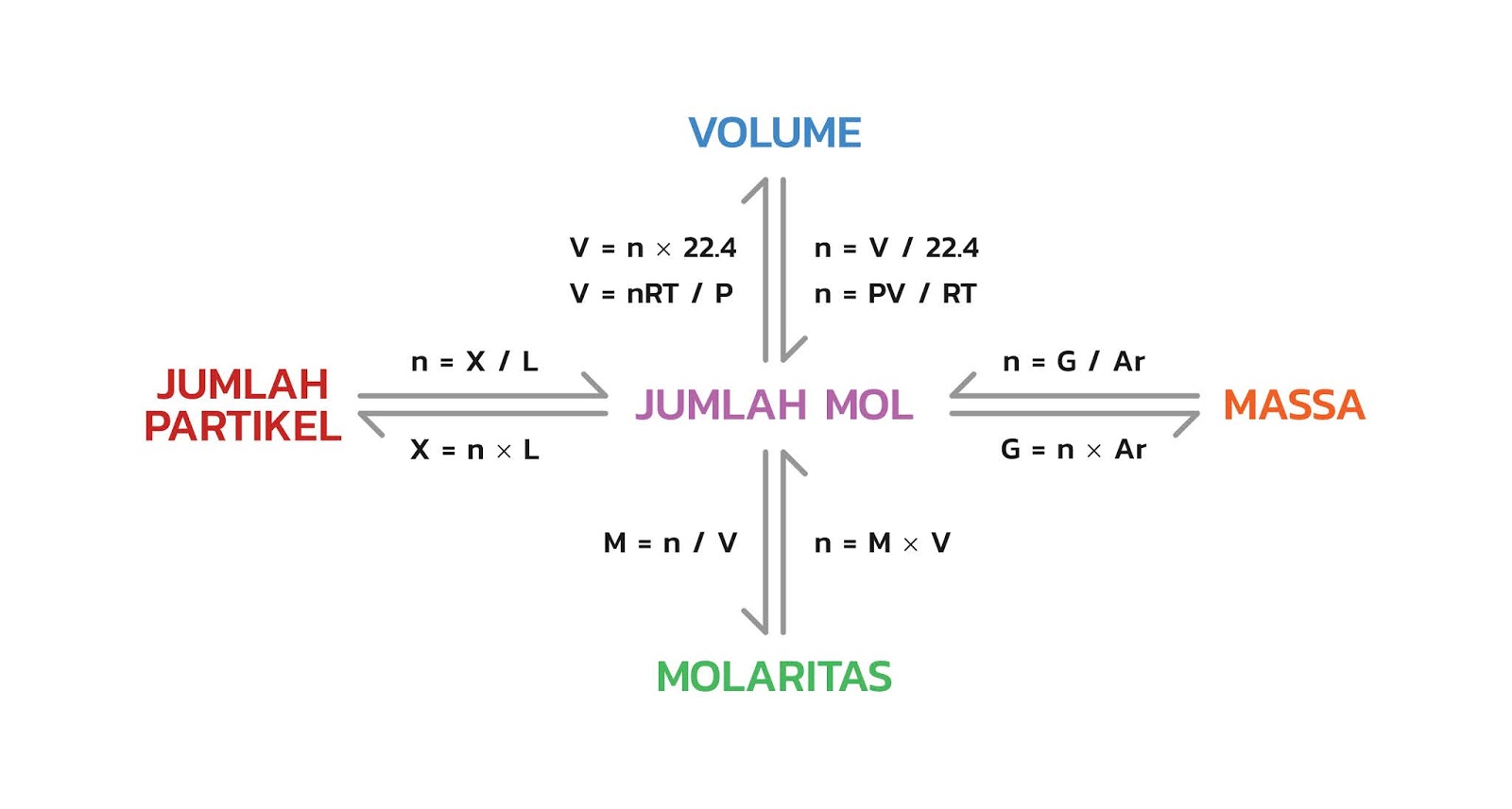
Hubungan Mol Dengan Jumlah Partikel Massa Volume Dan Molaritas Riset
Rumus Molaritas. Molaritas ini merupakan jenis konsentrasi larutan yang dipengaruhi oleh sifat koligatif larutan, yaitu molaritas, molalitas, dan fraksi mol.. Berapa molaritas larutan asam sulfat 25% (massa) dengan massa jenis 1,178 g/mL dan M adalah 98. Pembahasan: Misalnya massa larutan = 100 gram. massa = 25% x 100 gr = 25 gram. n = m/M.

Hubungan molaritas, massa jenis larutan dan kadar zat YouTube
Rumus molekul air adalah H 2 O. Massa molekul natrium sulfat dihitung dengan: M=23×2+32+16×4=142. Artinya, jumlah mol natrium sulfat dalam soal yang diberikan dihitung dengan: n = 15/142. = 0,106. Volume larutannya adalah 125 ml, jika dinyatakan dalam satuan liter menjadi 0,125 L.
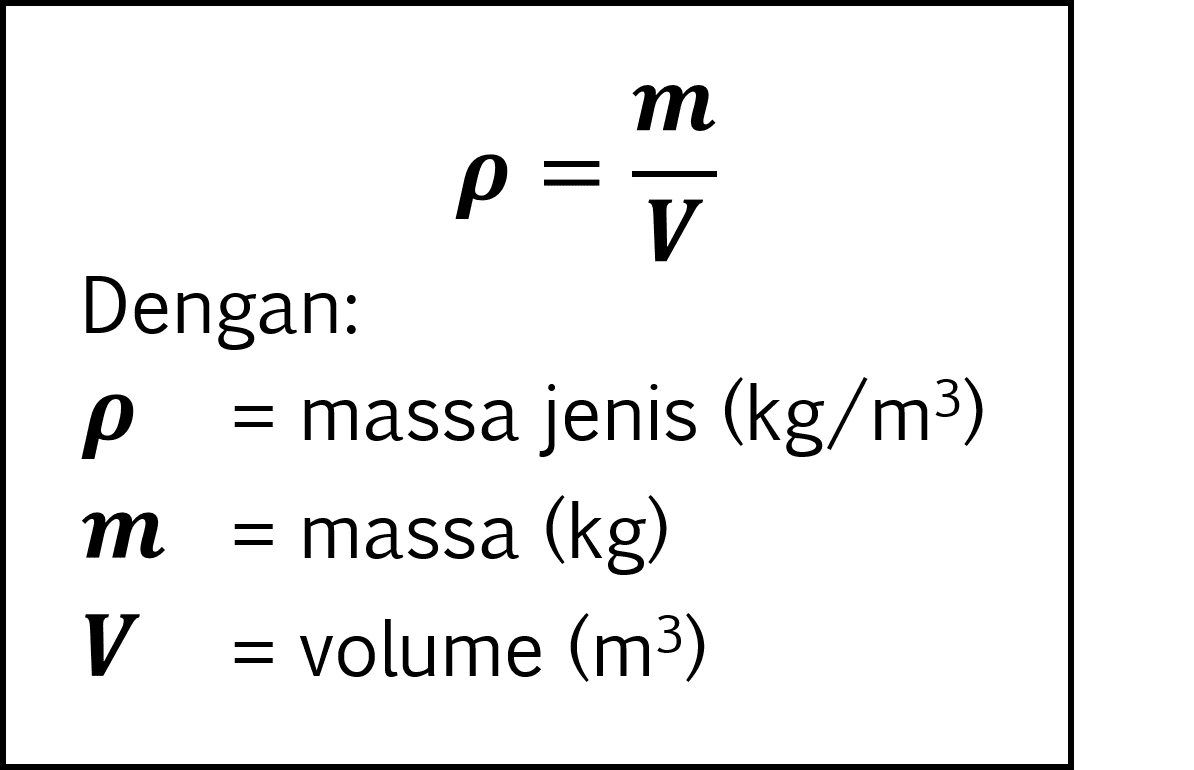
Rumus Massa Jenis Dalam Fisika Dan Contoh Soalnya Kumparan Com Gambaran
Rumus molaritas dengan massa jenis merupakan sebuah konsep penting dalam kimia yang digunakan untuk menghitung konsentrasi suatu larutan. Dengan rumus tersebut, massa jenis larutan dan bobot molekul larutan dapat diperoleh dengan mudah. Di dalam artikel ini, Anda akan mempelajari cara menggunakan rumus molaritas dengan massa jenis dan juga contoh perhitungan yang dapat membantu Anda memahami.
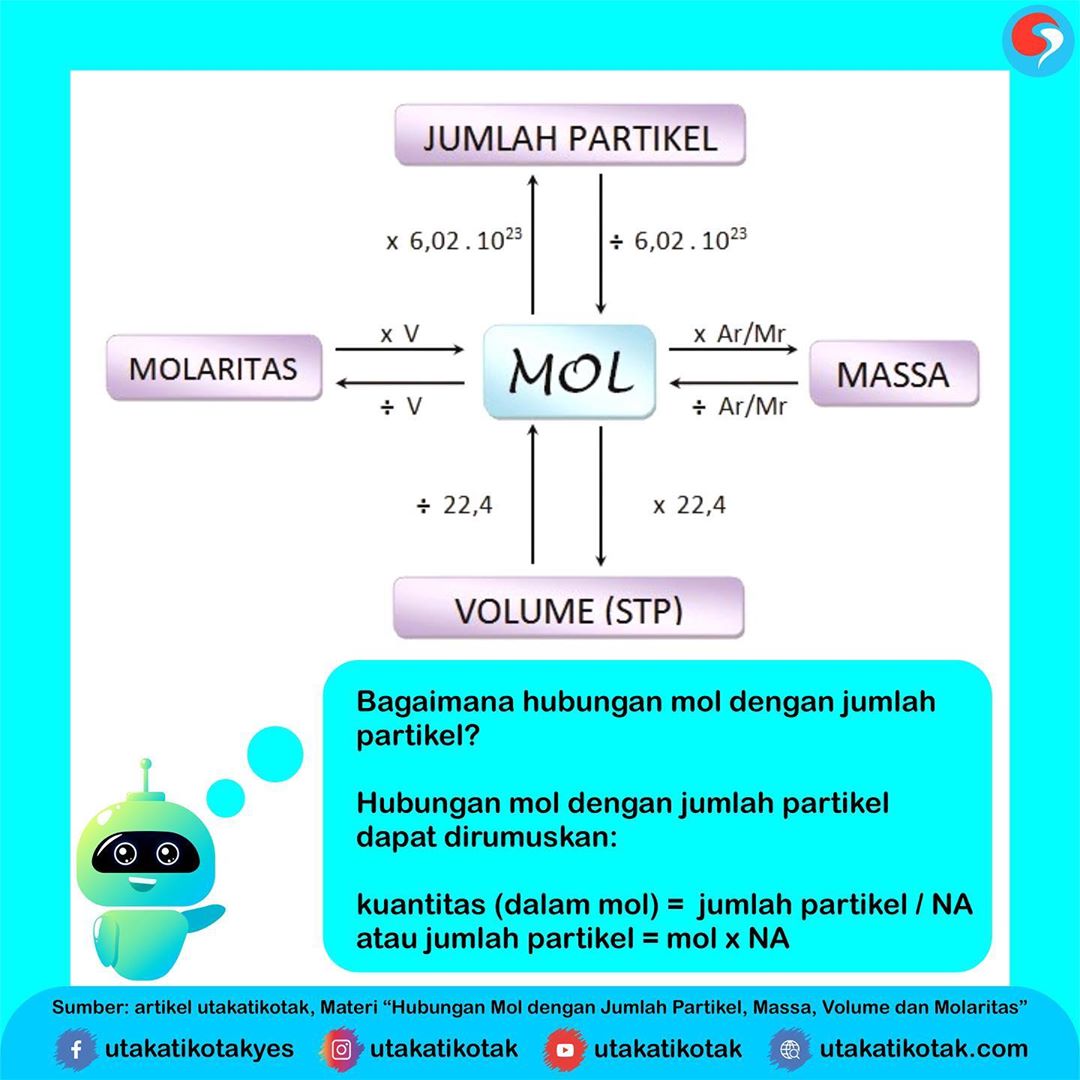
Hubungan Mol dengan Jumlah Partikel, Massa, Vo
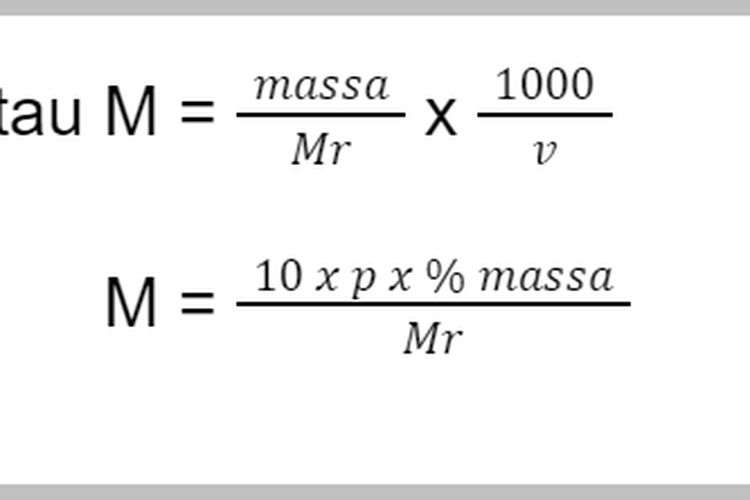
Sabtu, 27 Oktober 2018. Beberapa buku kimia terdapat rumus konversi satuan konsentrasi larutan dari kadar (a%), massa jenis (ρ, dibaca rho), dan data massa molar zat. Molaritas = a × ρ × 10 Massa molar mol/L. Dari manakah angka 10 pada rumus molaritas itu. Beberapa siswa tidak dapat menjelaskan asal muasal angka 10 itu.

Cara menghitung massa benda dan massa jenis benda dengan menggunakan Hukum Archimedes YouTube
4. Berapa molaritas larutan asam sulfat 25% (massa) dengan massa jenis 1,178 g/mL dan M r adalah 98? Diketahui: Misalkan massa larutan 100 gram, massa (H 2 SO 4) = 25% x 100 gr = 25 gram n(H 2 SO 4) = m / M r n(H 2 SO 4) = 25 / 98 = 0,255 mol. Ditanya: Molaritas larutan asam 25% (M)? Jawab: Untuk menentukan Molaritas, kita harus mencari volume.

Pengertian Rumus Dan Contoh Soal Mol Molalitas Molaritas Dan Riset My XXX Hot Girl
Soal dan Jawaban Konsentrasi Larutan: Molaritas, Molalitas, Fraksi Mol, Persen Berat, Normalitas. 1. Konversi molal ke % massa. Contoh soal: Hitunglah % massa dari larutan NaI 0,2 molal (massa molar NaI = 150 g/mol) Penyelesaian: Arti 0,2 molal NaI adalah 0,2 mol NaI dalam 1 Kg pelarut air. massa NaI sebanyak 0,2 mol = 0,2 mol x 150 g/mol = 30 g.
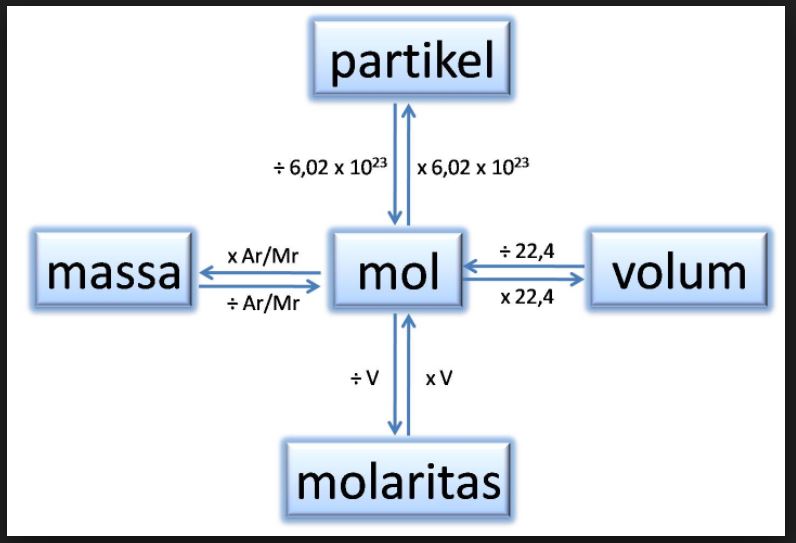
Hubungan Mol dengan Jumlah Partikel dan Massa Zat cekrisna
Untuk menghitung molaritas, kita dapat menggunakan rumus molaritas. Berikut adalah rumus-rumus molaritas! M = g/Mr x 1.000/V atau M = n/V. Dengan, M: molaritas (mol/L) n: jumlah mol zat g: massa zat terlarut (gram) Mr: massa molekul relatif zat terlarut (g/mol) V: volume larutan (mL) Baca juga: Soal UAS Kimia: Prinsip Molalitas dan Molaritas.

apa perbedaan molalitas dan molaritas Brainly.co.id
Massa jenis adalah pengukuran massa pada setiap satuan volume benda. Semakin tinggi nilai massa jenis suatu benda, maka semakin besar pula massa setiap volumenya. Satuan massa jenis dalam "CGS (centi - gram - sekon)" adalah: gram per sentimeter kubik (g/cm3). 3. Perbedaan antara Molalitas dengan Molaritas

Kimia 12 Molaritas Molalitas dan Fraksi Mol YouTube
Rumus molaritas Rumus yang digunakan untuk menghitung atau menentukan molaritas sebagai berikut: M = n V Jika yang akan dicari molaritasnya. g = massa (gram) Mr = Massa molekul relatif zat terlarut.. Tentukan molaritas larutan yang dibuat dengan melarutkan: 0,8 mol NaCl dalam 250 mL air;

Massa Jenis Pengertian, Rumus, Dan Satuan + Contoh Soalnya (LENGKAP)
Biasanya satuan molaritas ini ditandai dengan huruf M atau disebut juga Molar. Perlu diingat, bahwa huruf M yang dipakai adalah huruf M kapital. Nah, rumus konsentrasi larutan berdasarkan satuan molaritas adalah sebagai berikut. Keterangan: M = molaritas zat (molar) n = mol suatu zat (mol) V = volume larutan (liter)

Cara mudah menentukan massa zat dari molaritas YouTube
Beberapa satuan konsentrasi itu antara lain : mol, molalitas, molaritas, normalitas, ppm, persen massa, persen volum. Berikut akan saya jelaskan pengertian dan rumus dari satuan-satuan di atas : 1. Mol ( n ) Simbol satuan: n Mol adalah massa (gram) suatu zat dibagi dengan massa molekul relatif / berat molekul suatu zat. Rumus :

Molaritas asam nitrat pekat 63 dengan massa jenis 1,3 k...
Rumus normalitas, molaritas, molalitas sebenarnya saling memiliki keterkaitan antara satu sama lain. Molalitas dapat disimbolkan dengan huruf 'm; dan terdapat dua rumus molalitas yang bisa Grameds kuasai, yakni. Rumus Molalitas Dasar (Zat Pelarut n Kilogram) Molalitas = mol terlarut / kg pelarut ⇒ m = n / P.