
Contoh soal tingkat energi elektron
Itu adalah urutan tingkat energi kulit dan subkulit suatu atom. Ada 4 subkulit yaitu s, p, d, dan f dan angka sebelum subkulit menunjukkan kulit. Subkulit 1s punya tingkat energi paling rendah, lalu naik ke subkulit 2s, 2p, 3s, 3p, sampai terakhir yang paling tinggi 8s. Pastinya elektron yang bisa mengisi subkulit tertentu juga terbatas.

Jika jarijari elektron tingkat energi terendah pada mode...
Urutan energi orbital atom dari yang paling rendah ke yang paling tinggi adalah 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, dan seterusnya. Maka elektron akan menempati sub kulit 1s terlebih dahulu baru menempati sub kulit 2s. Pada subkulit s hanya dapat ditempati oleh 2 elektron. Pada subkulit p hanya dapat ditempati 6 elektron.

Cara Cepat Menuliskan Konfigurasi Elektron, Golongan, dan Periode YouTube
Urutan energi orbital atom dari energi yang paling rendah ke tingkat energi paling tinggi menggunakan prinsip aufbau. Adapun urutannya adalah ; 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p 8s Jadi dapat disimpulkan urutan penempatan elektron dari tingkat energi terendah yang benar adalah 1s 2s 2p 3s 3p 4s 3d 4p 5s.

Gambarkan Konfigurasi Elektron Untuk Atom Netral Tugas Sekolah
Konfigurasi Elektron dan Diagram Orbital; Urutan penempatan elektron dari tingkat energi terendah yang benar adalah.. Konfigurasi Elektron dan Diagram Orbital;. 4s 3p adalah.. Tonton video. Perhatikan pengisian elektron dalam orbital berikut!1) [A. Tonton video. Suatu unsur memiliki notasi 52 24Cr. Diagram orbital yang.
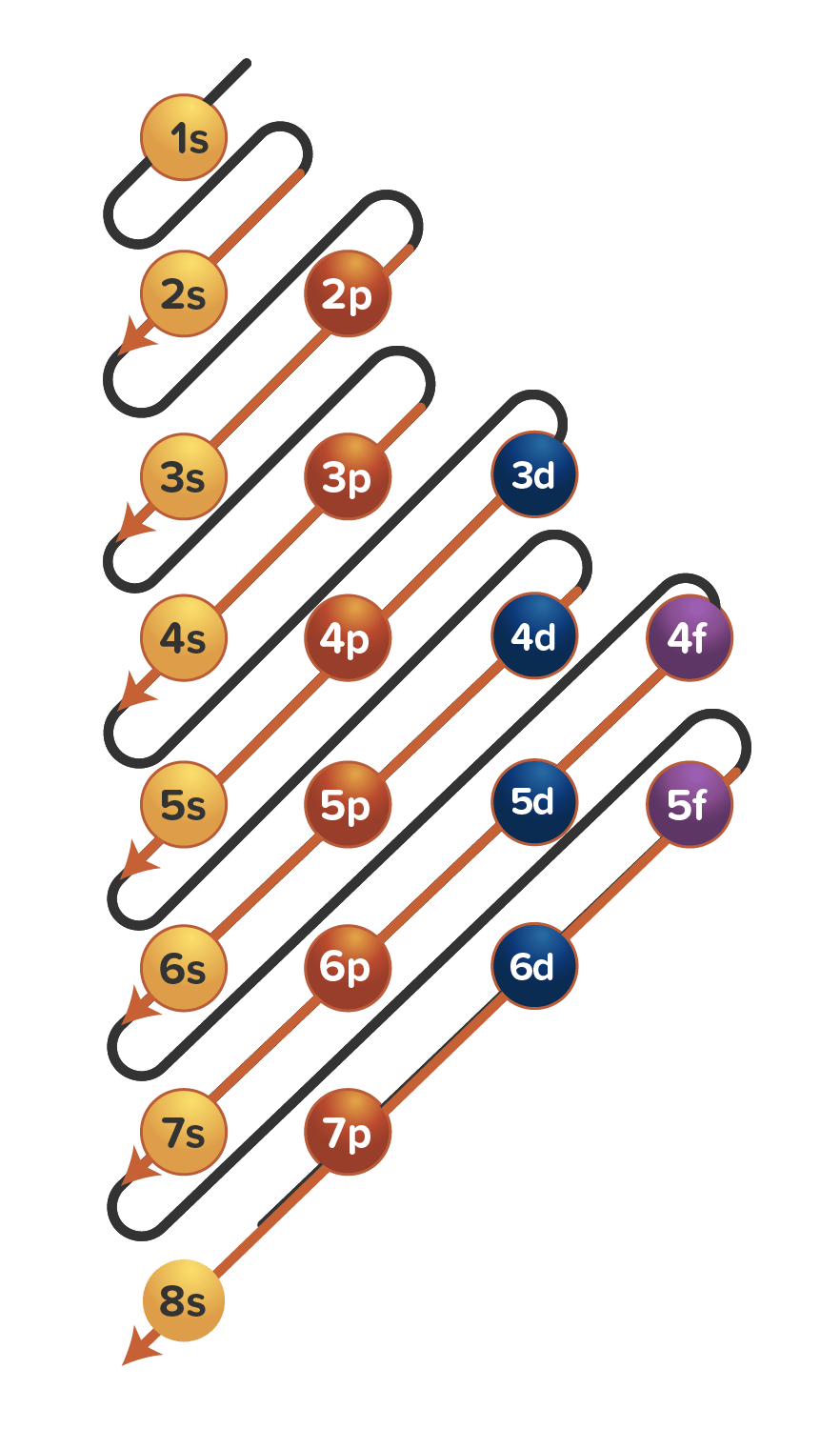
Perpindahan elektron yang disertai pelepasan energ...
Urutan di mana orbital diatur berdasarkan kenaikan energi sesuai dengan aturan Madelung. Setiap panah merah diagonal menyatakan nilai yang berbeda dari n + ℓ.. Prinsip Aufbau menyatakan bahwa, secara hipotetis, elektron yang mengorbit satu atau lebih atom mengisi tingkat energi terendah yang tersedia sebelum mengisi tingkat yang lebih tinggi (misalnya, 1s sebelum 2s).

Pengisian elektron dimulai dari tingkat energi terendah m...
Konfigurasi elektron menjadi salah satu materi yang ada dalam mata pelajaran kimia untuk kelas X (sepuluh) Sekolah Menengah Atas (SMA). Dalam kimia, konfigurasi elektron merupakan julukan untuk susunan elektron yang terbentuk pada kulit atom. Fungsi dari konfigurasi elektron adalah untuk menentukan sifat dan penempatan atom pada sistem periodik.

Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
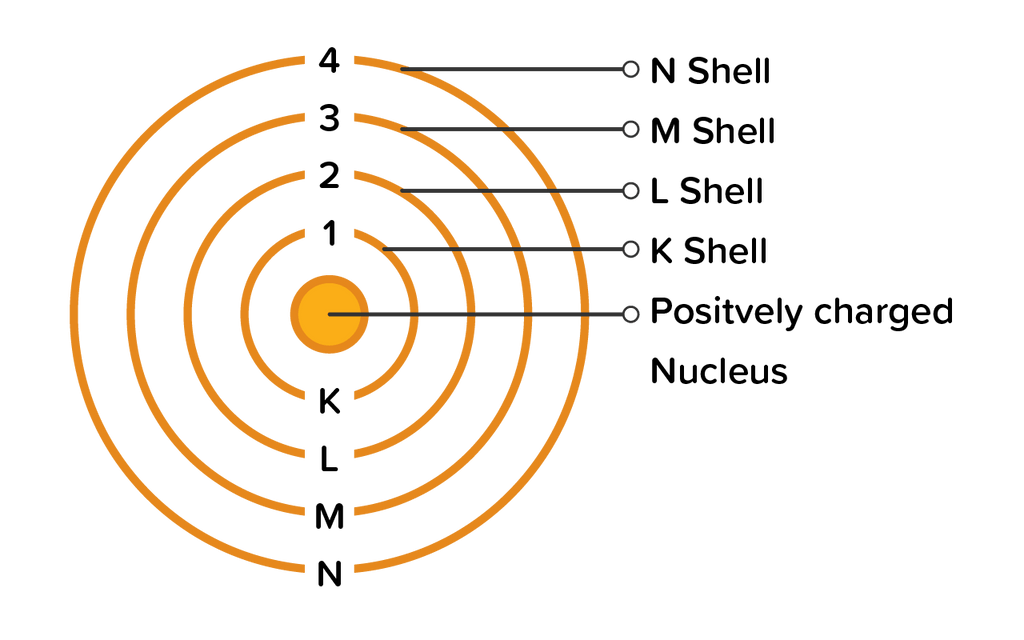
Pertama, jarak dan orbit yang ditekankan dalam model atom Bohr tidak sejalan dengan "Prinsip Ketidakpastian Heisenberg", yakni jarak/radius tak bisa bersama dengan orbit. Kedua, teori atom Bohr juga tidak mampu memberikan jawaban atas Efek Zeeman, yaitu efek yang ketika garis spectrum terbagi-bagi akibat adanya sebuah medan magnet.
Tentukan konfigurasi elektron dari 26 Fe
Konfigurasi elektron menurut Bohr merupakan pengisian elektron yang dimulai dari tingkat energi (kulit) yang paling rendah yaitu kulit K (kulit pertama, n = 1).. Urutan penempatan elektro dari tingkat energi terendah yang benar adalah.. A. 1s 2s 2p 3s 3p 3d 4s 4p 4d.. Untuk menentukan urutan pengisian elektron dalam atom, kita harus.
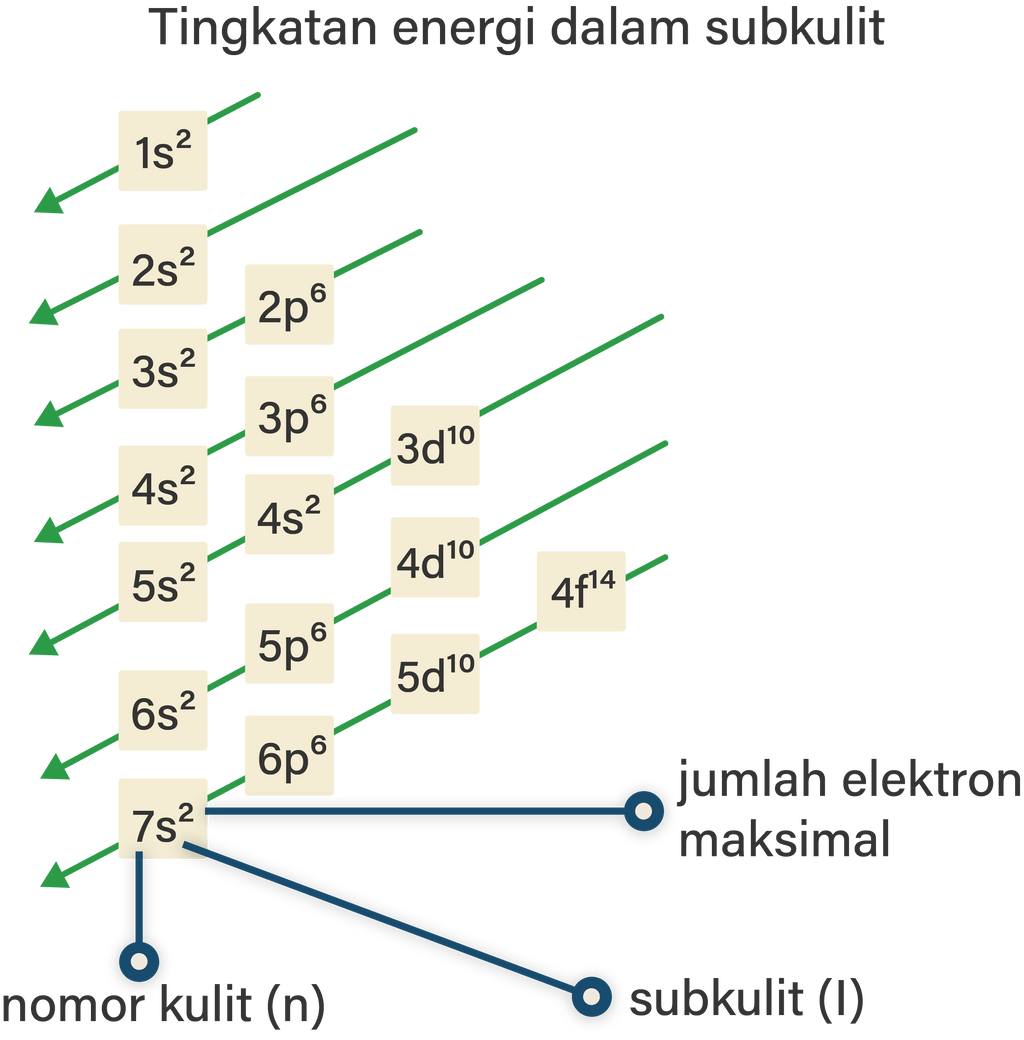
Jelaskan tentang konfigurasi elektron beserta cont...
Maka besarnya energi elektron pada lintasan ke n adalah: Jika nilai π = 3,14 , k = 9 × 10 9 Nm 2 /C 2, m = 9,1 × 10-31 kg, e = 1,6 × 10-19 C, h = 6,62 × 10-34 Js, dan 1 eV = 1,6 × 10-19 J kita dimasukkan dalam persamaan, maka didapatkan energi elektron pada suatu lintasan tertentu adalah : Tingkat Energi Elektron Untuk Melepaskan Ikatan

Hitunglah energi dari sebuah foton cahaya biru (lambda=4...
Jumlah elektron secara maksimal yang dapat ditempati pada setiap kulit yaitu kulit pertama (kulit K) memiliki 2 elektron, kulit kedua (kulit L) memiliki 8 elektron, kulit ketiga (kulit M) memiliki 18 elektron, dan kulit keempat (kulit N) memiliki 32 elektron. Urutan pengisian elektron dimulai dari kulit yang mempunyai tingkat energi terendah.

Urutan penempatan elektron dari tingkat energi terendah y...
Gambar 2: Urutan penempatan elektron dari tingkat energi terendah yang benar. Urutan penempatan elektron dalam atom dapat dilihat pada tabel periodik. Tabel periodik merupakan susunan unsur-unsur kimia berdasarkan urutan peningkatan nomor atomnya. Dalam tabel ini, elektron-elektron diatur secara sistematis mengikuti pola urutan penempatan elektron.

Contoh Soal Konfigurasi Elektron Beserta Pembahasannya
Urutan tingkat energi dari tingkat energi yang rendah ke tingkat energi yang lebih tinggi digambarkan sebagai diagram elektron Aufbau, yaitu 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s. Oleh karena itu, cara pengisian elektron yang tepat pada tingkat energi sesuai urutan adalah 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s. Jadi, jawaban yang benar adalah D.

PPT MODEL ATOM PowerPoint Presentation, free download ID1996005
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Urutan penempatan elektr.
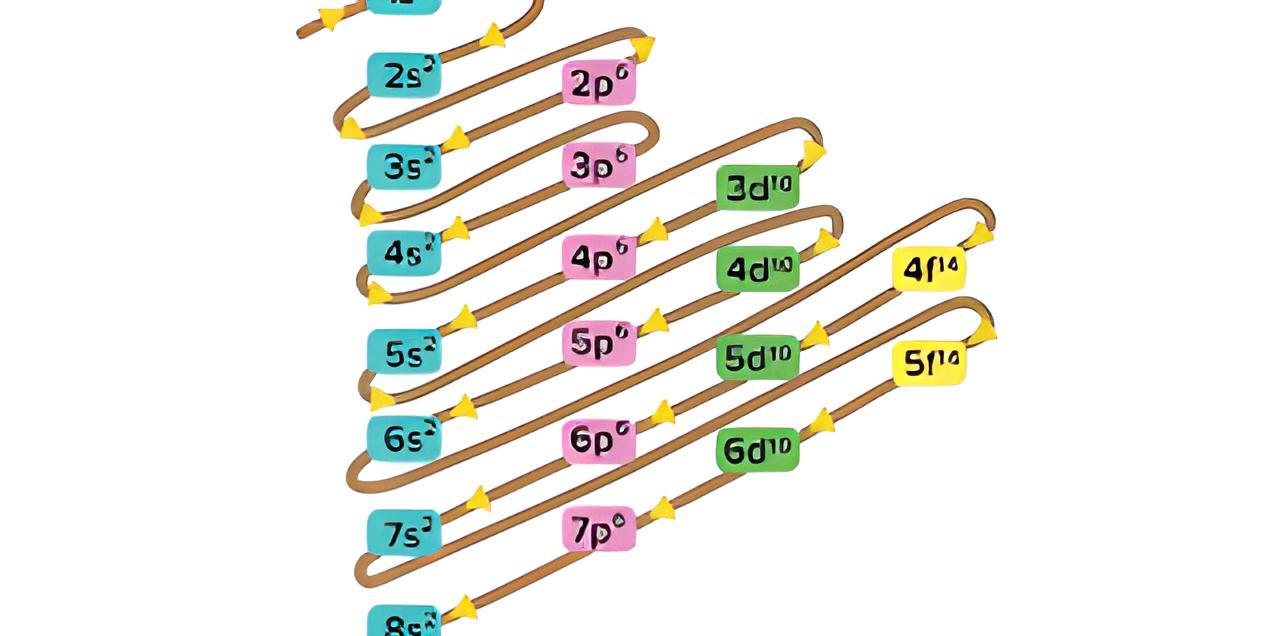
Aturan Konfigurasi Elektron Dan Diagram Orbital Superprof
Beranda » Umum » Urutan penempatan elektron dari tingkat energi terendah yang benar adalah. Urutan penempatan elektron dari tingkat energi terendah yang benar adalah. 2024-02-16 oleh admin. Urutan penempatan elektron dari tingkat energi terendah yang benar adalah. 1s 2s 2p 3s 3p 3d 4s 4p 4d; Kedua; Ketiga; Ke empat; Kelima;
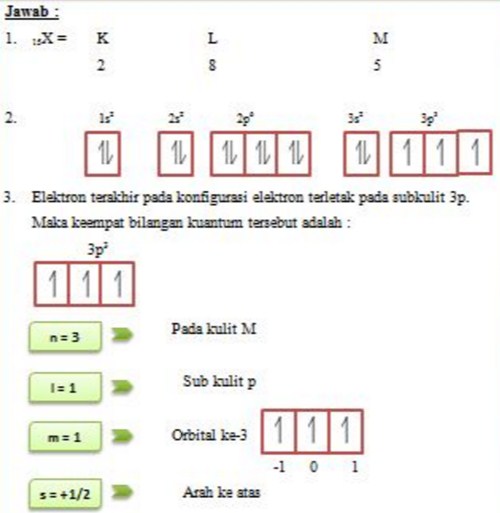
Konfigurasi Elektron Menurut Larangan Pauli Rumus Kimia
Urutan penempatan elektron dari tingkat energi terendah yang benar adalah 1s 2s 2p 3s 3p 4s 3d 4p 5s. Pembahasan dan Penjelasan Jawaban A. 1s 2s 2p 3s 3p 3d 4s 4p 4d menurut saya kurang tepat, karena kalau dibaca dari pertanyaanya jawaban ini tidak nyambung sama sekali.
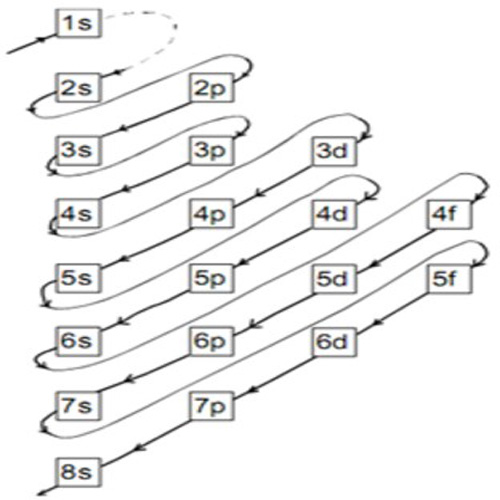
Pengertian Konfigurasi Elektron Rumus Kimia
Aturan penentuan konfigurasi elektron berdasarkan orbital: 1. Asas Aufbau: Elektron menempati orbital-orbital dimulai dari tingkat energi yang terendah, dimulai dari 1s, 2s, 2p, dan seterusnya seperti urutan subkulit yang terlihat pada Gambar 2. Gambar 2. Urutan tingkat energi subkulit.